在下列物质中:
④CH3-C≡C-CH2-CH3 ⑤2—甲基-1,3-戊二烯 ⑥甲基环戊烷
⑦1,4—二甲基苯 ⑧ ⑨
⑨
属于同系物的是 ,属于同种物质的是 ,属于同分异构体的是 。
由环己烷可制得1, 4 – 环己二醇,下列有7步反应(其中无机产物都已略去),其中有②步属于消去反应,③步属于加成反应。试回答: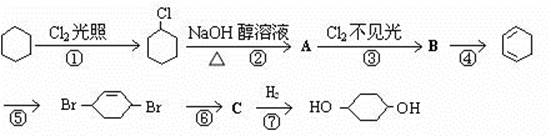
(1)反应属于取代反应。
(2)化合物的结构简式:B,C;
(3)反应④所用试剂和条件是;
(4)写出反应②、⑤的化学方程式:
反应②
反应⑤
(16分)聚苯乙烯的结构为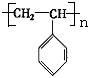 ,试回答下列问题:
,试回答下列问题:
(1)聚苯乙烯的链节是_________________,单体是___________________;
(2)实验测得聚苯乙烯的相对分子质量(平均值)为52000,则该高聚物的聚合度n为_________。
(3)已知聚苯乙烯为线性结构的高分子化合物,试推测:_________(“能”与“不能”)溶于CHCl3,具有__________(填“热塑”或“热固”)性。
某课外研究小组,用含有较多杂质的铜粉,通过不同的化学反应制取胆矾。其设计的实验过程为: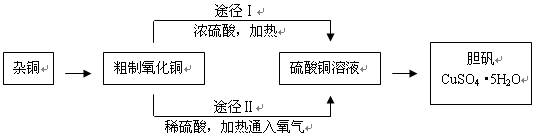
(1)铜中含有大量的有机物,可采用灼烧的方法除去有机物,灼烧是将瓷坩埚置于上(用以下所给仪器编号填入,下同),取用坩埚应使用,灼烧后的坩埚应放在上,不能直接放在桌面上。
实验所用仪器:a.蒸发皿 b.石棉网 c.泥三角 d.表面皿 e.坩埚钳 f.试管夹
(2)杂铜经灼烧后得到的产物是氧化铜及少量铜的混合物,用以制取胆矾。灼烧后含有少量铜的可能原因是()(填字母编号,有两个选项符合题意。)
a.灼烧过程中部分氧化铜被还原 b.灼烧不充分铜未被完全氧化
c.氧化铜在加热过程中分解成铜 d.该条件下铜无法被氧化
(3)由粗制氧化铜通过两种途径制取胆矾,与途径Ⅰ相比途径Ⅱ有明显的两个优点:
、
(本题12分)有机物A是一种重要化工生产的中间体,其结构简式为:C6H5-CH2CH(OH)COOH
(1)A中含有的官能团有:、(填名称)。
(2)A可能具有的化学性质有:(填序号)
①能与H2发生加成反应;②能与在烧碱溶液中发生水解反应;③能与甲酸发生酯化反应;④能金属钠发生反应,且有机物A与反应生成的氢气物质的量之比为1∶1反应;⑤能与Ag(NH3) 2OH溶液发生银镜反应。
(3)写出A分别与乙醇、乙酸发生酯化反应的方程式:
。
(4)在催化剂Pt的作用下,A与H2加成后的生成物的结构简式为。
元素在周期表中的位置,反映了元素的原子结构和元素性质。下图是元素周期表的一部分。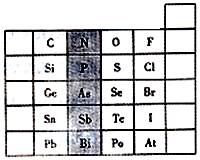
(1)阴影部分中元素N在元素周期表中的位置为第周期族,其单质分子中含有的共用电子对数目为对。
(2)根据元素周期律,请你预测H3AsO4、H3PO4、
的酸性强弱:H3AsO4H3PO4(填“>”、“<”或“=”)。
(3)在一定条件下,S、Se都能与H2反应,根据元素周期律判断,Se与H2反应比S与H2的反应。(填“更难”或“更易”)