在恒温恒容的密闭容器中进行反应A(g)=B(g)+C(g),若反应物浓度由1 mol·L-1降到0.6 mol·L-1需要20s,则反应物浓度再由0.6 mol·L-1降到0.4 mol·L-1所需要的时间为:
| A.10s | B.大于10s | C.小于10s | D.无法判断 |
设NA表示阿伏加得德罗常数的数值,下列叙述中正确的是
| A.0.2 mol/L的Ba(NO3)2溶液1L,含NO3-数为0.2NA |
| B.常温常压下,22.4L氧气所含的原子数为2NA |
| C.常温常压下,48gO2、O3组成的混合气体所含的氧原子数为3NA |
| D.1L 0.1mol/LNaCl溶液中所含的Na+的电子数为1.1NA |
下列从混合物中分离出其中的某一成分,所采取的分离方法正确的是
| A.利用氯化钾与碳酸钙的溶解性差异,可用溶解、过滤的方法除去碳酸钙 |
| B.由于碘在酒精中的溶解度大,所以可用酒精把碘水中的碘萃取出来 |
| C.水的沸点是100 ℃,酒精的沸点是78.5 ℃,所以可用加热蒸馏法使含水酒精变为无水酒精 |
| D.氯化钠的溶解度随温度的下降而减小,所以可用冷却法从热的含有少量氯化钾的氯化钠浓溶液中得到纯净的氯化钠晶体 |
下列仪器常用于物质分离的是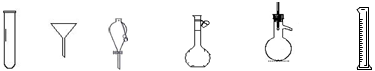
①②③④⑤⑥
| A.①③⑤ | B.①②⑥ | C.②④⑤ | D.②③⑤ |
下列实验中,①pH试纸的使用,②过滤,③蒸发,④配制一定物质的量浓度溶液,均用到的仪器是
| A.蒸发皿 | B.玻璃棒 | C.试管 | D.分液漏斗 |
质量分数为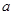 %的NaOH溶液蒸发掉b g水后,得到V mL质量分数为2
%的NaOH溶液蒸发掉b g水后,得到V mL质量分数为2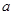 %的NaOH溶液,则蒸发后NaOH溶液的物质的量浓度为
%的NaOH溶液,则蒸发后NaOH溶液的物质的量浓度为
A.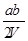 mol/L mol/L |
B.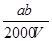 mol/L mol/L |
C.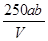 mol/L mol/L |
D.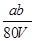 mol/L mol/L |