某兴趣小组根据金属镁与C02的反应,推测金属钠也能与C02发生反应,因此
他们用下图所示的装置进行“钠与C02反应”的探究(尾气处理装置略去).又知实
验过程中的C02气体为足量;设能发生的反应都进行完全;一氧化碳气体可用氯化钯
(PdCl2)溶液来检验(通过溶液颜色的变化来判断)。
(1)为了使制取气体的装置能“随开随用,随关随停”,则在图中A处应选用的装置是 (填“I”、“Ⅱ”或“Ⅲ”).若要用干燥、纯净的C02气体与金属钠反应,则装置B中应盛放的试剂是 溶液。
(2)实验开始,检查装置的气密性完好并装入有关药品后,在点燃酒精喷灯前,还必须进行的实验操作是 。
(3)反应完成后,装置D玻璃管中残留的固体物质可能是 。(填字母) .Na202 b.Na2C03 c.NaHCO3 d.Na2C03和C
.Na202 b.Na2C03 c.NaHCO3 d.Na2C03和C
(4)若D玻璃管中残留的固体是纯净物,则钠与C02反应的化学方程式是 。
(5)请设计合理的实验来检验某固体物质是Na2C03.答: 。
“柯达尔”是一种高聚物,其结构式为:
已知在一定条件下可以发生如下反应: -CH3+Cl2→
-CH3+Cl2→ -CH2Cl+HCl
-CH2Cl+HCl
以石油产品(对二甲苯)为原料,合成“柯达尔”的方案如下:
回答以下问题:
(1)指出反应的类型:
A→B:______________________,A→E:______________________。
(2)写出下列反应的化学方程式:
B→C:
E→F:
D+F→柯达尔: 。
有机物甲的结构简式如下,它可通过不同的化学反应分别制得结构简式为乙~庚的物质.
请回答下列问题:
(1)指出反应的类型:
甲→丙:______________________,甲→丁:______________________。
(2)在甲~庚七种物质中,互为同分异构体的是_____________________。(填代号,下同);可看作酯类的是、和庚。
(3)已知HCHO分子中所有原子都在同一平面内,则在上述分子中所有原子有可能都在同一平面内的物质是______________________。
化学反应经常伴随着颜色变化,下列有关反应获得的颜色正确的是
(多选扣分)
①天然蛋白质遇浓硝酸→黄色 ②淀粉溶液遇碘化钾→蓝色
③新制Cu(OH)2与乙醇共热→红色④热的氧化铜遇乙醇→绿色
⑤苯酚溶液中加FeCl3溶液→紫色⑥苯酚在空气中氧化→粉红色
在2L密闭容器内,800℃时反应:2NO(g)+O2(g) 2NO2(g)体系中,n(NO)随时间的变化如下表:
2NO2(g)体系中,n(NO)随时间的变化如下表:
| 时间(s) |
0 |
1 |
2 |
3 |
4 |
5 |
| n(NO)(mol) |
0.020 |
0.010 |
0.008 |
0.007 |
0.007 |
0.007 |
(1)NO的平衡浓度c(NO)=。
(2)图中表示NO2变化的曲线是。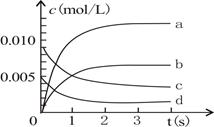
(3)能说明该反应已达到平衡状态的是。
a.v(NO2)=2v(O2)
b.容器内气体总物质的量保持不变
c.v逆(NO)=2v正(O2)
d.容器内气体的密度保持不变
X、Y、Z、W、L、M六种短周期主族元素的原子序数依次增大,其中X、M的单质在常温下呈气态,Y的原子最外层电子数是其电子层数的2倍,Z在同周期的主族元素中原子半径最大,W是地壳中含量最多的金属元素,L的单质晶体熔点高、硬度大,是一种重要的半导体材料。
用化学用语回答下列问题:
(1)L的元素符号为___________;M在元素周期表中的位置为__________________。
(2)Y、L、M的最高价含氧酸的酸性由弱到强的顺序是_________________________。
(3)Y的最高价氧化物的电子式为__________。原子序数比Y多2的元素的一种氢化物能分解为它的另一种氢化物,此分解反应的化学方程式是_________________。
(4)R与Y同周期,R的单质分子R2中有3个共价键,R与L能形成一种新型无机非金属材料,其化学式是___________________。