城市使用的燃料,现大多为煤气、液化石油气。煤气的主要成分是CO和H2的混合气体,它有煤炭与水蒸气在高温下反应制得,故又称水煤气。试回答:
(1)写出制取水煤气的主要化学方程式 ,该反应是 反应(填吸热、放热)。
(2)设液化石油气的主要成分为丁烷(C4H10),其充分燃烧后产物为C02和H2O,试比较
完全燃烧等质量的C4H10及CO所需的氧气的质量比(结果保留1位小数)。
 以黄铁矿为原料生产硫酸的工艺流程图如下:
以黄铁矿为原料生产硫酸的工艺流程图如下:

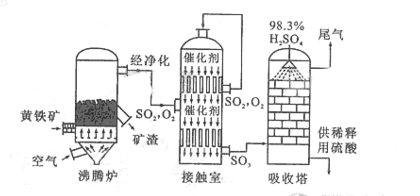

 (1)将燃烧黄铁矿的化学方程式补充完整
(1)将燃烧黄铁矿的化学方程式补充完整 4+11
4+11
 (2)接触室中发生反应的化学方程式是。
(2)接触室中发生反应的化学方程式是。 (3)依据工艺流程图判断下列说法正确的是(选填序号字母)。
(3)依据工艺流程图判断下列说法正确的是(选填序号字母)。 a. 为使黄铁矿充分燃烧,需将其粉碎
a. 为使黄铁矿充分燃烧,需将其粉碎 b. 过量空气能提高
的转化率
b. 过量空气能提高
的转化率 c. 使用催化剂能提高
的反应速率和转化率
c. 使用催化剂能提高
的反应速率和转化率 d. 沸腾炉排出的矿渣可供炼铁
d. 沸腾炉排出的矿渣可供炼铁 (4)每160g
气体与
(4)每160g
气体与 化合放出260.6
的热量,该反应的热化学方程是。
化合放出260.6
的热量,该反应的热化学方程是。
(5)吸收塔排出的尾气先用氨水吸收,再用浓硫酸处理,得到较高浓度的
和铵盐。 ①
既可作为生产硫酸的原料循环再利用,也可用于工业制溴过程中吸收潮湿空气中的
。
吸收
的离子方程式是。
①
既可作为生产硫酸的原料循环再利用,也可用于工业制溴过程中吸收潮湿空气中的
。
吸收
的离子方程式是。 ② 为测定该铵盐中氮元素的质量分数,将不同质量的铵盐分别加入到50.00
相同浓度的
溶液中,沸水浴加热至气体全部逸出(此温度下铵盐不分解)。该气体经干燥后用浓硫酸吸收完全,测定浓硫酸增加的质量。
② 为测定该铵盐中氮元素的质量分数,将不同质量的铵盐分别加入到50.00
相同浓度的
溶液中,沸水浴加热至气体全部逸出(此温度下铵盐不分解)。该气体经干燥后用浓硫酸吸收完全,测定浓硫酸增加的质量。 部分测定结果;
部分测定结果; 铵盐质量为10.00
和20.00
时,浓硫酸增加的质量相同;铵盐质量为30.00
时,浓硫酸增加的质量为0.68
;铵盐质量为40.00
时,浓硫酸的质量不变。
铵盐质量为10.00
和20.00
时,浓硫酸增加的质量相同;铵盐质量为30.00
时,浓硫酸增加的质量为0.68
;铵盐质量为40.00
时,浓硫酸的质量不变。 计算:该铵盐中氮元素的质量分数是%; 若铵盐质量为15.00
。 浓硫酸增加的质量为。 (计算结果保留两位小数)
计算:该铵盐中氮元素的质量分数是%; 若铵盐质量为15.00
。 浓硫酸增加的质量为。 (计算结果保留两位小数)
丙烯可用于合成是杀除根瘤线虫的农药(分子式为
)和应用广泛的
树脂;


 已知脂与酯克发生如下酯交换反应:
已知脂与酯克发生如下酯交换反应: (
代表羟基)
(
代表羟基) (1)农药
分子中每个碳原子上均连有卤原子。
(1)农药
分子中每个碳原子上均连有卤原子。 ①
的结构简式是
①
的结构简式是 含有的官能团名称是;
含有的官能团名称是; ②由丙烯生成A的反应类型是
②由丙烯生成A的反应类型是 (2)
水解可得到
,该水解反应的化学方程式是。
(2)
水解可得到
,该水解反应的化学方程式是。 (3)
蒸汽密度是相同状态下甲烷密度的6.25倍,
中各元素的质量分数分别为碳60%,氢8%,氧32% ,
的结构简式是。
(3)
蒸汽密度是相同状态下甲烷密度的6.25倍,
中各元素的质量分数分别为碳60%,氢8%,氧32% ,
的结构简式是。 (4)下列说法正确的是(选填序号字母)
(4)下列说法正确的是(选填序号字母) a.能发生聚合反应,还原反映和氧化反映
a.能发生聚合反应,还原反映和氧化反映 b.
含有两个甲基的羟酸类同分异构体有4个
b.
含有两个甲基的羟酸类同分异构体有4个 c
催化加氢的产物与B具有相同的相对分子质量
c
催化加氢的产物与B具有相同的相对分子质量 d E有芳香气味,易溶于乙醇
d E有芳香气味,易溶于乙醇 (5)
的水解产物经分离子最终的到甲醇和
,二者均可循环利用
树脂的制备。其中将甲醇与
分离的操作方法是
(5)
的水解产物经分离子最终的到甲醇和
,二者均可循环利用
树脂的制备。其中将甲醇与
分离的操作方法是 (6)
的分子式为
单体为苯的二元取代物,且两个取代基部处于对位,该单体苯环上的一溴取代物只有两种。D和F反应生成
单体的化学方程式。
(6)
的分子式为
单体为苯的二元取代物,且两个取代基部处于对位,该单体苯环上的一溴取代物只有两种。D和F反应生成
单体的化学方程式。
下图表示有关物质(均由短周期元素形成)之间的转化关系,其中
为常见的金属单质,
为非金属单质(一般是黑色粉末),
是常见的无色无味液体,
是淡黄色的固体化合物。(反应条件图中已省略。)

 (1)
、
、
、
代表的物质分别为、、、(填化学式);
(1)
、
、
、
代表的物质分别为、、、(填化学式); (2)反应①中的
、
均过量,该反应的化学方程式是;
(2)反应①中的
、
均过量,该反应的化学方程式是; (3)反应②中,若
与
物质的量之比为4∶3,
分别是、(填化学式);
(3)反应②中,若
与
物质的量之比为4∶3,
分别是、(填化学式); (4)反应③产物中
的化学式为;
(4)反应③产物中
的化学式为; (5)反应④的离子方程式为。
(5)反应④的离子方程式为。
均为有机化合物,它们之间的转化如下图所示:

实验表明:①
既能发生银镜反应,又能与金属钠反应放出氢气: ②核磁共振氢谱表明
分子中有三种氢,且其峰面积之比为1:1:1;
②核磁共振氢谱表明
分子中有三种氢,且其峰面积之比为1:1:1; ③
能使溴的四氯化碳溶液褪色;④1
与足量金属钠反应可放出22.4
氢气(标准状况)。
③
能使溴的四氯化碳溶液褪色;④1
与足量金属钠反应可放出22.4
氢气(标准状况)。 请根据以上信息回答下列问题:
请根据以上信息回答下列问题: (1)
的结构简式为(不考虑立体结构),由
生成
的反应类型是反应;
(1)
的结构简式为(不考虑立体结构),由
生成
的反应类型是反应; (2)
的结构简式为;
(2)
的结构简式为; (3)由
生成
的化学方程式为,
中官能团有(填名称),与
具有相同官能团的
的同分异构体还有(写出结构简式,不考虑立体结构);
(3)由
生成
的化学方程式为,
中官能团有(填名称),与
具有相同官能团的
的同分异构体还有(写出结构简式,不考虑立体结构); (4)
的结构简式为;
(4)
的结构简式为; (5)由
(5)由 生成
的化学方程式。
生成
的化学方程式。
 已知
、
和
三种元素的原子序数之和等于42。
元素原子的4
轨道上有3个未成对电子,
元素原子的最外层2
轨道上有2个未成对电子。
跟
可形成化合物
,
元素可以形成负一价离子。请回答下列问题:
已知
、
和
三种元素的原子序数之和等于42。
元素原子的4
轨道上有3个未成对电子,
元素原子的最外层2
轨道上有2个未成对电子。
跟
可形成化合物
,
元素可以形成负一价离子。请回答下列问题: (1)
元素原子基态时的电子排布式为,该元素的符号是;
(1)
元素原子基态时的电子排布式为,该元素的符号是; (2)
元素原子的价层电子的轨道表示式为,该元素的名称是;
(2)
元素原子的价层电子的轨道表示式为,该元素的名称是; (3)
与
可形成化合物
,该化合物的空间构型为;
(3)
与
可形成化合物
,该化合物的空间构型为; (4)已知化合物
在稀硫酸溶液中可被金属锌还原为
,产物还有
和
,该反应的化学方程式是_;
(4)已知化合物
在稀硫酸溶液中可被金属锌还原为
,产物还有
和
,该反应的化学方程式是_; (5)比较
的氢化物与同族第二、第三周期元素所形成的氢化物稳定性、沸点高低并说明理由。
(5)比较
的氢化物与同族第二、第三周期元素所形成的氢化物稳定性、沸点高低并说明理由。