二甲醚(CH3OCH3)是一种重要的清洁燃料,也可替代氟利昂作制冷剂等,对臭氧层无破坏作用.工业上可利用煤的气化产物(水煤气)合成二甲醚.
请回答下列问题:
(1)煤的气化过程中产生的有害气体H2S用Na2CO3溶液吸收,生成两种酸式盐,该反应的化学方程式为:_____ _____.
(2)利用水煤气合成二甲醚的三步反应如下:
①2H2(g)+CO(g)═CH3OH(g);△H=﹣90.8kJ•mol﹣1
②2CH3OH(g)═CH3OCH3(g)+H2O(g);△H=﹣23.5kJ•mol﹣1
③CO(g)+H2O(g)═CO2(g)+H2(g);△H=﹣41.3kJ•mol﹣1
总反应:3H2(g)+3CO(g)═CH3OCH3(g)+CO2(g) △H=___________;则该反应( )
| A.任何温度下都能进行 |
| B.任何温度下都不能进行 |
| C.高温下能自发进行 |
| D.低温下能自发进行 |
一定条件下的密闭容器中,该总反应达到平衡,要提高CO的转化率,可以采取的措施是__________(以上都填字母代号).
a.高温高压 b.加入催化剂 c.减少CO2的浓度
d.增加CO的浓度 e.分离出二甲醚
(3)已知反应②2CH3OH(g)═CH3OCH3(g)+H2O(g)某温度下的平衡常数为400.此温度下,在密闭容器中加入CH3OH,反应到某时刻测得各组分的浓度如下:
| 物质 |
CH3OH |
CH3OCH3 |
H2O |
| 浓度/(mol•L﹣1) |
0.44 |
0.6 |
0.6 |
①比较此时正、逆反应速率的大小:v正__________ v逆 (填“>”、“<”或“=”).
②若加入CH3OH后,经10min反应达到平衡,此时c(CH3OH)=__________.
[化学—选修2化学与技术](15分)
空气吹出法工艺是目前“海水提溴”的最主要方法之一,其工艺流程如下:
(1)目前,从海水中提取的溴约占世界溴年产量的。
(2)步骤①中用硫酸酸化可提高Cl2的利用率,其原因是。
(3)步骤④的离子方程式为。
(4)步骤⑥的蒸馏过程中,溴出口温度要控制在80〜90℃。温度过高或过低都不利于生产,理由是。
(5)步骤⑧中溴蒸气冷凝后得到液溴与溴水的混合物,可利用它们的相对密度相差较大的特点进行分离。分离仪器的名称是,分离时液溴从分离器(填“上口”或“下口")排出。
(6)不直接用含溴的海水进行蒸馏得到液溴,而要经过“空气吹出、S02吸收、氯化”的原因是。
(7)某同学测得苦卤中溴的含量为0.8g/L,已知步骤①〜⑥中溴共损失了25%,步骤⑦和步骤⑧又共损失了所得溴蒸气的10%,若处理10 m3这样的苦卤,可得到液溴mol。
(14分)铁是地壳中含量第二的金属元素,其单质、合金及化合物在生产生活中的应用广泛。
(一)工业废水中含有一定量的Cr2O72-和CrO42-,它们会对人类及生态系统产生很大的危害,必须进行处理。常用的处理方法是电解法,该法用Fe作电极电解含Cr2O72-的酸性废水,随着电解的进行,阴极附近溶 液pH升高,产生Cr(OH)3沉淀。
(1)用Fe作电极的目的是。
(2)阴极附近溶液pH升高的原因是(用电极反应式解释)溶液中同时生成的沉淀还有。
(二)氮化铁磁粉是一种磁记录材料,利用氨气在4000C以上分解得到的氮原子渗透到高纯铁粉中可制备氮化铁。制备高纯铁粉涉及的主要生产流程如下:

已知:①某赤铁矿石含60.0% Fe2O3、3.6% FeO,还含有A12O3、MnO2、CuO等。
②部分阳离子以氢氧化物形式完全沉淀时溶液的pH如下:
(3)步骤②中加双氧水的目的是,pH控制在3. 4的作用是。已知25°C时, ,该温度下反应:Cu2++2H2O
,该温度下反应:Cu2++2H2O Cu(OH)2+2H+的平衡常数K=。
Cu(OH)2+2H+的平衡常数K=。
(4)如何判断步骤③中沉淀是否洗涤干净?
(5)制备氮化铁磁粉的反应: (未配平),若整个过程中消耗氨气34.0 g,消耗赤铁矿石2 kg,设整个过程中无损耗,则氮化铁磁粉的化学式为。
(未配平),若整个过程中消耗氨气34.0 g,消耗赤铁矿石2 kg,设整个过程中无损耗,则氮化铁磁粉的化学式为。
Ⅰ.A、B、C、D、E为五种常见的短周期元素,常温下,A、B可形成B2A2和B2A两种液态化合物,B与D可组成分子X,X水溶液呈碱性,C元素的焰色反应呈黄色,E与C同周期,且E的最高价氧化物的水化物呈两性。试回答:
(1)D元素在周期表中的位置为;
(2)由A、D、E三种元素形成的盐的水溶液呈酸性,用离子方程式解释其原因;
(3)用A单质和B单质可制取气体燃料电池,该电池用多孔的惰性电极浸入浓KOH溶液,两极分别通入A单质和B单质。写出该电池负极的电极反应式:。
Ⅱ.将20mLpH=2的NaHSO4溶液逐滴加入到20mL 0.1mol·L-1Na2CO3溶液中,向此反应后的溶液中滴加0.001 mol·L-1BaCl2溶液,首先析出的沉淀是。[KSP(BaSO4)=1.1×10-10mol2·L-2;KSP(BaCO3)=5.1×10-9mol2·L-2]
Ⅲ.某温度下在容积固定的密闭容器中,下列反应达到平衡:M(g)+H2O(g) N(g)+H2(g)
N(g)+H2(g)
| n(M):n(H2O) |
M转化率 |
H2O转化率 |
| 1:1 |
0.5 |
0.5 |
| 1:2 |
0.67 |
0.33 |
| 1:3 |
0.75 |
0.25 |
①该反应的平衡常数为_____。该温度下,向容器中充入1molM、3mol H2O、2mol N、1.5molH2,则起始时该反应速率V正____V逆(填“>”、“<”或“=”)
②结合表中数据判断下列说法中正确的是。
A.增加H2O(g)的量,M的转化率升高而H2O(g)的转化率降低
B.若M与H2O(g)的转化率相同时,二者的初始投入量一定相同
C.M和H2O(g)初始物质的量之比等于二者转化率之比
D.当M与H2O(g)物质的之比为1:4时,M的转化率为0.85
【化学——选修:化学反应原理;必做题】
为有效控制雾霾,各地积极采取措施改善大气质量.有效控制空气中氮氧化物、碳氧化物和硫氧化物显得尤为重要。
(1)在汽车排气管内安装催化转化器,可将汽车尾气中主要污染物转化为无毒的大气循环物质。
已知:①N2(g)+O2(g)=2NO(g)△H1=+180.5kJ/mol
②C和CO的燃烧热(△H)分别为-393.5kJ·mol-1和-283kJ·mol-1。
则2NO(g)+2CO(g)=N2(g)+2CO2(g)的△H=______________kJ·mol-1
(2)将0.20 molNO和0.10 molCO充入一个容积为1L的密闭容器中,反应过程中物质浓度变化如图所示。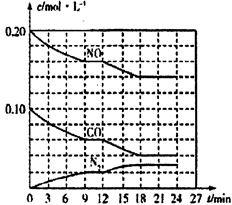
①0-9min内的平均反应速率v(N2)=_____mol· L-1·min-1(保留两位有效数字);第12 min时改变的反应条件可能为______________。
| A.升高温度 | B.加入NO | C.加催化剂 | D.降低温度 |
②该反应在第24 min时达到平衡状态,CO2的体积分数为__________(保留三位有效数字),化学平衡常数K=___________(保留两位有效数字)。
(3)烟气中的SO2可用某浓度NaOH溶液吸收得到Na2SO3和NaHSO3混合溶液,且所得溶液呈中性,该溶液中c(Na+)=____________(用含硫微粒浓度的代数式表示)。
(4)通过人工光合作用能将水与燃煤产生的CO2转化成HCOOH和O2.已知常温下0.1 mol·L-1的HCOONa溶液pH=10,则HCOOH的电离常数Ka=___________。
已知在溶液中IO3-与I-、I2与S2O32-有如下反应:
IO3-+5I-+6H+=3I2+3H2O I2+2S2O32-=2I-+S4O62-
某课外活动小组为测定混有MgCl2的食用加碘盐中所含MgCl2、KIO3的含量,按下图所示实验步骤进行实验.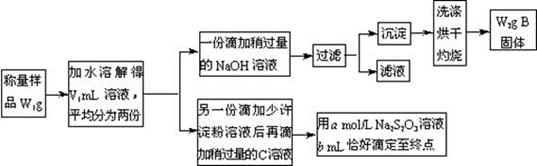
请回答下列问题:
(1)写出B和C的化学式:B________________,C________________。
(2)加入NaOH溶液必须稍过量的原因是________________________________。
(3)过滤用到的玻璃仪器有__________________________________________。
(4)该滴定实验所需仪器有下列中的_____________(填序号)
A.酸式滴定管
B.碱式滴定管
C.量筒
D.锥形瓶
E.铁架台
F.滴定管夹
G.烧杯
H.白纸
I.胶头滴管
J.漏斗
滴定时,判断滴定达到终点的现象是____________________________。
(5)MgCl2的质量分数是__________________________________________,KIO3的质量分数是_______________________________(列出计算式,可不化简)。
(6)使所测MgCl2的质量分数可能偏高的操作是_____________(填写字母)
A.过滤后未洗涤所得沉淀,直接烘干灼烧
B.在敞口容器中用托盘天平称量样品时,操作时间过长
C.沉淀灼烧不彻底