最近科学家提出“绿色自由”构想:把空气吹入碳酸钾溶液,然后再把CO2从溶液中提取出来,经化学反应后使之变为可再生燃料甲醇。“绿色自由”构想技术流程如下: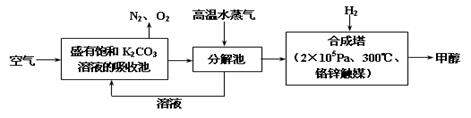
(1)上述流程中碳酸钾溶液所起的作用是: ;
(2)分解池中反应的化学方程式为 ;
(3)在合成塔中,若有4.4 kg CO2与足量H2恰好完全反应,生成气态的水和甲醇气体,可放出4947 kJ
的热量,试写出合成塔中发生反应的热化学方程式:
;
(4)从平衡移动原理分析,低温有利于原料气的转化,实际生产中采用300℃的高温,原因之一是考虑到催化剂的催化活性,原因之二是 ;
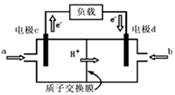
(5)右图是甲醇燃料电池的结构示意图。甲醇在催化剂作用下提供质子(H+)和电子,电子经外电路、质子经内电路到达另一极与氧气反应,电池总反应为:2CH3OH + 3O2=2CO2 + 4H2O则:a处通进的物质是 (写名称);电极d的名称是 极;电极c处发生的电极反应方程为: 。
甲、乙分别是两种主族元素形成的氧化物,它们广泛存在于地壳中,均不溶于水,且都有如下相 同的转化关系,不同之处是乙对应的转化过程中需控制盐酸用量,若盐酸过量则得不到白色沉淀B。
同的转化关系,不同之处是乙对应的转化过程中需控制盐酸用量,若盐酸过量则得不到白色沉淀B。
(1) 写出甲、乙的化学式:甲________,乙________;
(2) 写出下列反应的化学方程式:
甲+NaOH溶液____________________________________________,
乙+NaOH溶液____________________________________________;
(3) 分别写出甲、乙对应的A溶液与过量盐酸反应的离子方程式:
甲 ________________________________________
乙______________ ______________________________
______________________________
(4) 若将5.1g乙溶于适量的盐酸(二者恰好完全反应)后,再加入175 mL的2 mol.L-1NH3H2O溶液,得到沉淀___________g
常温下,用 0.1000 mol L-1NaOH溶液滴定 20.00 ml0.1000 mol.L-1CH3COOH溶液,所得滴定曲线如下图所示。
请回答:
(1) 有人认为,C点时NaOH与CH3COOH恰好完全反应,这种看法是否正确______?(选填“是”或“否”),理由是________________________;
(2) 关于该滴定实验,从下列选项中选出最恰当的一项____ (选填字母);
(3) 在B点时,溶液中 ________
________ (选填“>”、“<”或“=”);
(选填“>”、“<”或“=”);
(4) 在A〜D区间内,下列大小关系可能存在的是________;
①
②
③
④
(5) 若向该醋酸溶液中加入少量的醋酸钠晶体,则溶液的pH会____(选填“增大”、“减小”或“不变”);
(6) 常温下,用该NaOH溶液滴定25.00 mL—定浓度的某稀H2SO4溶液,达到滴定终点时消耗NaOH溶液的体积为25.00 mL,则该稀H2SO4溶液的pH=____。
有一种融雪剂,其主要成分的化学式为XY2, X、Y均为周期表前20号元素,其阳离子和阴离子的电子层结构相同,且1 molXY2含有54 mol电子.
(1)该融雪剂的化学式是;Y与氢元素形成的化合物的电子式是。
(2)元素D.E原子的最外层电子数是其电子层数的2倍,D与Y相邻,则D原子的电子排布式;D与E能形成一种非极性分子,该分子的立体构型名称为。
(3)元素W与Y同周期,其单质是原子晶体;元素Z的单质分子Z2中有3个共价健;W与Z能形成一种新型无机非金属材料,其化学式是。
(14分)(Ⅰ)、某一反应体系有反应物和生成物共五种物质:O2、H2CrO4、Cr(OH)3、H2O、H2O2
已知该反应中H2O2只发生如下过程:H2O2→ O2
(1)写出该反应的化学方程式________________________。
(2)该反应中的还原剂是;还原产物是____________。
(Ⅱ)四只试剂瓶中分别盛装有NaNO3溶液、Na2CO3溶液、Na2SO4溶液和NaCl溶液,就如何检验这四种溶液分别解答下列各题。
在四支试管中分别取四种溶液各1mL,做下列实验。
(1)在四支试管中分别滴入,出现 现象的,是,
现象的,是,
(2)在剩余三支试管中分别滴入,出现现象的,是,
(3)在剩余两支试管中分别滴入,出现现象的,是,三次实验中都没有明显现象的是。
下图每一方框中的字母代表一种反应物或生成物: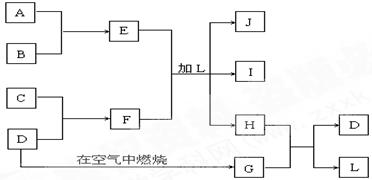
产物J是含A金属元素的胶状白色沉淀,可由E与氨水反应制取。I为氯化钠溶液,D是淡黄色固体单质。试填写下列空白:
(1)F的化学式为 :_________________。
:_________________。
(2)L的化学式为:______________。
(3)写出J受热分解反应的化学方程式:____________________。
(4)H和G之间反应的化学方程式为:________________________。
(5) E与氨水反应的离子方程式_______________________。