随着经济的不断发展,人们对环境问题也越来越关注。
(1)室内空气污染问题得到越来越多的关注,下列物质中也属于室内挥发性有机污染物的是
___________________。(填字母)
a.苯 b.甲烷 c.醋酸 d.乙烯
(2)下列措施中,有利于降低室内污染物浓度的是__________。(填字母)
a.勤开窗通风 b.日常生活中利用天然气替代煤作燃料
c.使用“绿色环保”装饰材料 d.室内放一些活性碳
(3) “温室效应”是全球关注的环境问题之一。CO2是目前大气中含量最高的一种温室气体。因此,控制和治理CO2是解决温室效应的有效途径。将CO2转化成有机物可有效实现碳循环。CO2转化成有机物的例子很多,如:
a.6CO2 + 6H2O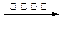 C6H12O6+6O2 b.CO2 + 3H2
C6H12O6+6O2 b.CO2 + 3H2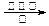 CH3OH +H2O
CH3OH +H2O
c.CO2 + CH4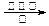 CH3COOH d.2CO2 + 6H2
CH3COOH d.2CO2 + 6H2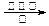 CH2==CH2 + 4H2O
CH2==CH2 + 4H2O
以上反应中,最节能的是 ,原子利用率(原子利用率=期望产物的总质量与生成物的总质量之比)最高的是 。
(4) “汽车尾气污染”已倍受世人关注。以辛烷(C8H8)代表汽油的成分,要使辛烷正好完全燃烧,则辛烷气与空气(空气中O2占1/5体积)的体积比(相同条件下)为 (保留三位小数)。
金属钒(V)在材料科学上有重要作用,被称为“合金的维生素”。在测定矿石中钒的含量时有如下操作: 用已知浓度的硫酸酸化的H2C2O4溶液,滴定(VO2)2SO4溶液。
(1)完成滴定过程的离子反应方程式,方框内填数字,短线上填物质的化学式或离子符号。
VO2+ +H2C2O4 + ______→VO2+ +CO2 + ______
(2)当收集到标准状况下气体11.2升时,电子转移的数目为
(6分) 某透明澄清溶液可能含有Na+、Fe3+、Ba2+、CO32-、SO32-、SO42-、Cl-、I-等离子中的几种,为鉴别这些离子,分别取三份少量溶液,按照以下顺序进行三个实验:
实验①:加CCl4,再滴加少量氯水,振荡后,CCl4层变为紫色;
实验②:加盐酸后,生成无色无味气体,该气体能使饱和石灰水溶液变浑浊;
实验③:加BaCl2溶液产生白色沉淀,过滤出沉淀,在沉淀中加入足量盐酸,沉淀不能完全溶解。
(1)分析上述3个实验,用离子符号写出每一个实验得出的结论,可不必完全填满。
实验①:含有;不含;
实验②:含有;不含;
实验③:含有;不含;(可不必完全填满)
(2)通过上述实验,不能确定是否存在的离子是。
写出下列化学方程式或离子方程式。
(1)钠与氧气在常温下反应;化学方程式____________________________________。
(2)实验室多余氯气的尾气吸收;离子方程式______________________________。
(3)漂白粉的作用原理,与H2O和CO2作用;化学方程式______________________________。
(4)氢氧化铁加热分解;化学方程式________________________。
(5)次氯酸光照分解;化学方程式____________________________________。
(6)铁丝在氯气中燃烧;化学方程式__________________________________。
(7)三氯化铁溶液与铁粉反应;离子方程式________________________。
(8)新制氢氧化亚铁遇空气被氧化成氢氧化铁;化学方程式___________________________。
(9)加热碳酸氢钙溶液产生白色沉淀;化学方程式___________________________________。
(10)碳酸氢钠溶液与氢氧化钠溶液混合;化学方程式________________________________。
生态农业涉及农家肥料的综合利用。某种肥料经发酵得到一种含有甲烷、二氧化碳、氮气的混合气体8.96L(标准状况)。该气体通过盛有红色CuO粉末的硬质玻璃管,发生的反应为:CH4+4CuO CO2↑+2H2O↑+4Cu。当甲烷完全反应后,硬质玻璃管的质量减轻了4.8g。将反应后气体通入2L 0.1mol/L的澄清Ca(OH)2溶液,充分吸收,生成沉淀10g。
CO2↑+2H2O↑+4Cu。当甲烷完全反应后,硬质玻璃管的质量减轻了4.8g。将反应后气体通入2L 0.1mol/L的澄清Ca(OH)2溶液,充分吸收,生成沉淀10g。
(1) 原混合气体的物质的量是____________;生成沉淀的摩尔质量是____________。
(2) 原混合气体中甲烷的体积是____________。
(3) 求原混合气体中氮气的体积。
(第3小题请列式计算)
在花瓶中加入“鲜花保鲜剂”,能延长鲜花的寿命。下表是500mL“鲜花保鲜剂”中含有的成分,阅读后回答下列问题:
| 成分 |
质量(g) |
摩尔质量(g ·mol-1) |
| 蔗糖 |
25.00 |
342 |
| 硫酸钾 |
0.25 |
174 |
| 阿司匹林 |
0.17 |
180 |
| 高锰酸钾 |
0.25 |
158 |
| 硝酸银 |
0.02 |
170 |
(1)下列“鲜花保鲜剂”的成分中,属于非电解质的是________。
A.蔗糖 B.硫酸钾 C.高锰酸钾 D.硝酸银
(2)下列选项中,符合“鲜花保鲜剂”中K+(阿司匹林中不含K+)的物质的量浓度的试算式的是。
A.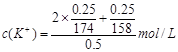
B. .
.
C.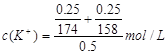
D.
(3)配制上述“鲜花保鲜剂”所需的仪器有:烧杯、玻璃棒、药匙、________________、______________、_______________。(在横线上填写所缺仪器的名称)
(4)在溶液配制过程中,下列操作对配制结果没有影响的是___________。
A.定容时仰视容量瓶刻度线
B.容量瓶在使用前未干燥,里面有少量蒸馏水
C.容量瓶在使用前刚刚配制完一定物质的量浓度的NaCl溶液而未洗净
D.定容摇匀后发现液面低于容量瓶的刻度线,但未做任何处理