氨在国民经济中占有重要地位。请回答有关氨的下列问题:
(1)已知:N2(g)+O2(g)=2NO(g) △H=+akJ/mol
4NH3(g)+5O2(g)=4 NO(g)+6H2O(g) △H=-bkJ/mol
NO(g)+6H2O(g) △H=-bkJ/mol
2H2(g)+O2(g)=2H20(g) △H=-ckJ/mol 则N2(g)+3H2(g) 2NH3(g)的△H= ;
则N2(g)+3H2(g) 2NH3(g)的△H= ;
(2)在一定温度下,将3molN2气体和7molH2气体通入到体积为1L的密闭容器中。当反应达到平衡时,容器内气体的压强为起始时的80%,则其平衡常数为 。改变下列条件,能使平衡向正反应方向进行且平衡常数不变的是 ;
①增大压强 ②增大反应物质的浓度
③使用催化剂 ④降低温度
(3)可以用氯气来检验输送氨气的管道是否漏气,如果漏气则会有白烟(成份为氯化铵)生成。该反应的化学方程式为 ;
(4)工业生产氨水的物质的量浓度为20mol/L,实验室若需用80mL浓度为5mol/L的氨水时,需取20mol/L的氨水 mL(用100mL的容量瓶)。假如该氨水的pH=a,加入相同体积的盐酸时,两溶液恰好反应,则此盐酸的pH 14-a(填“大于”“小于”或“等于”)。
利用15N可以测定亚硝酸盐对地下水质的污染情况。
(1)下列说法正确的是________。
| A.14N与15N为同种核素 |
| B.14N的第一电离能小于14C |
| C.15NH3与14NH3均能形成分子间氢键 |
| D.CH315NH2与CH3CH214NH2互为同系物 |
(2)15N的价层电子排布图为________;15NH4Cl的晶胞与CsCl相同,则15NH4Cl晶体中15NH4+的配位数为________;15NH4+中15N的杂化轨道类型为________。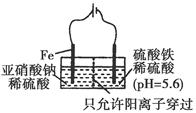
(3)工业上电解法处理亚硝酸盐的模拟工艺如图。已知阳极区发生化学反应:
2NO2—+8H++6Fe2+=N2↑+6Fe3++4H2O
①阳极电极反应方程式是________(不考虑后续反应);
②若硫酸溶液浓度过大,阴极区会有气体逸出,该气体为_______
(填化学式);该现象表明c(H+)越大,H+氧化性越________;
③若电解时电路中有0.6 mol电子转移,且NaNO2有剩余,则电解池中生成Na2SO4________mol。
A、B两元素,A的原子序数为x,A、B所在周期元素的种类分别为m和n,若A、B同在第ⅠA族,当B在A的上周期时,B的原子序数为________,当B在A的下周期时,B的原子序数为________;若A、B同在第ⅦA族,当B在A的上周期时,B的原子序数为________,当B在A的下周期时,B的原子序数为________。
元素周期表中前7周期的元素种类如下表所示:
| 周期数 |
一 |
二 |
三 |
四 |
五 |
六 |
七 |
| 元素种类 |
2 |
8 |
8 |
18 |
18 |
32 |
32 |
(1)第六、七周期比第四、五周期多了14种元素,其原因是_________________________________________。
(2)周期表中_______族所含元素最多,_______族元素形成化合物最多。
(3)请分析周期数与元素种类的关系,然后预言第八周期最多可能含有的元素种类为()
A.18 B.32
C.50 D.64
(4)居里夫人发现的镭是元素周期表中第七周期第ⅡA族元素,下列关于镭的性质的描述中不正确的是()
A.在化合物中呈+2价
B.氢氧化物呈两性
C.单质能使水分解,放出氢气
D.碳酸盐难4溶于水
元素周期表是学习和研究化学的重要工具。下列是元素周期表的部分信息: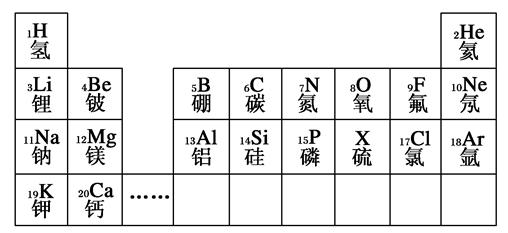
(1)地壳中含量最多的金属元素的原子序数是________。
(2)分析上表规律,可推知,表中X为________。
(3) 表示的是(写粒子符号)________。
表示的是(写粒子符号)________。
(4)写出一个由1、7、17号三种元素组成的化合物的化学式:________________________________________________________________________。
A、B、C为短周期元素,在周期表中所处的位置如图所示。A、C两元素的原子核外电子数之和等于B原子的质子数。B原子核内质子数和中子数相等。
(1)A、B、C三种元素的名称分别为__________、________、________。
(2)B位于元素周期表中第________周期第________族。
(3)C的原子结构示意图为________,C的单质与H2反应的化学方程式为_______________________________________________________________________。
(4)写出A的气态氢化物与B的最高价氧化物对应水化物反应的化学方程式__________________________________________________________。