高铁电池是一种新型可充电电池,与普通高能电池相比,该电池能长时间保持稳定的放电电压。高铁电池的总反应为
下列叙述不正确的是
| A.放电时每转移3 mol电子,正极有1mol K2FeO4被氧化 |
B.充电时阳极反应为:Fe(OH)3 —3e— + 5 OH— = FeO + 4H2O + 4H2O |
| C.放电时负极反应为:Zn—2e— +2OH—= Zn(OH)2 |
| D.放电时正极附近溶液的碱性增强 |
一定量的盐酸跟过量的铁粉反应时,为了减缓反应速率,且不影响生成氢气的总量,可向盐酸中加入适量的( )
①NaOH固体 ②H2O ③NaCl固体 ④CH3COONa固体 ⑤KCl溶液
| A.①② | B.②③⑤ | C.②④ | D.②④⑤ |
某学生的实验报告所列出的下列数据中合理的是( )
| A.用10mL量筒量取7.13mL稀盐酸 |
| B.用25mL滴定管做中和滴定实验时,用去某浓度的碱溶液21.70mL |
| C.用广泛pH试纸测得某溶液的pH为2.3 |
| D.用托盘天平称量25.20g NaCl |
现有X(g)+Y(g) 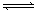 2Z(g);正反应放热。从反应开始经过t1后达到平衡状态,t2时由于条件改变,平衡受到破坏,在t3时又达到平衡,据下图回答:从t2→t3的曲线变化是由哪种条件引起的()
2Z(g);正反应放热。从反应开始经过t1后达到平衡状态,t2时由于条件改变,平衡受到破坏,在t3时又达到平衡,据下图回答:从t2→t3的曲线变化是由哪种条件引起的()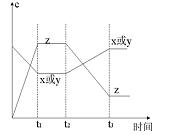
| A.增大X或Y的浓度 |
| B.增大压强 |
| C.增大Z的浓度 |
| D.升高温度 |
对于溶液的酸碱性说法正确的是()
| A.c(H+)很小的溶液一定呈碱性 | B.pH等于7的溶液一定呈中性 |
| C.c(H+)=c(OH-)的溶液一定呈中性 | D.不能使酚酞试液变红的溶液一定呈酸性 |
在恒温恒压的条件下,一密闭容器内发生反应:2NO2(g) 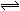 N2O4(g),达平衡时,再向容器内通入一定量的NO2(g),重达平衡后,与第一次平衡时相比,NO2的体积分数()
N2O4(g),达平衡时,再向容器内通入一定量的NO2(g),重达平衡后,与第一次平衡时相比,NO2的体积分数()
| A.不变 | B.增大 | C.减小 | D.无法判断 |