有A、B、C、D四块金属片,进行如下实验:
①A、B用导线相连后,同时浸入稀硫酸溶液中,A极为负极;
②C、D用导线相连后,同时浸入稀硫酸 溶液中,电流由D→导线→C;
溶液中,电流由D→导线→C;
③A、C相连后,同时浸入稀硫酸溶液中,C极产生大量气泡;
④B、D相连后,同时浸入稀硫酸溶液中,D极发生氧化反应。
据此,判断四种金属的活动性顺序是 ( )
A.A>B>C>D B.A>C>D>B C.C>A>B>D D.B>D>C>A
过氧乙酸是在抗SARS病毒期间常使用的一种高效杀毒剂,其分子式为C2H4O3,它具有氧化性,漂白作用,下列物质中漂白作用原理与过氧乙酸不同的是()
| A.氯水(次氯酸) | B.臭氧 | C.活性炭 | D.过氧化钠 |
苏丹红是很多国家禁止用于食品生产的合成色素。结构简式如图。关于苏丹红说法错误的是()
_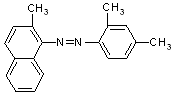
| A.分子中含一个苯环和一个萘环 | B.属于芳香烃 |
| C.能被酸性高锰酸钾溶液氧化 | D.能溶于苯 |
1 L水中溶有Mg(HCO3)2和CaCl2的浓度分别为b mol/L和2b mol/L,请在下列试剂中选用最合适的一种试剂把溶液中的Mg2+、Ca2+去掉( )
| A.NaHCO3 | B.Na2CO3 | C.NaOH | D.Ca(OH) 2 |
在一定条件下,将CO和O2的混合气体26g充入一体积固定不变的密闭容器(容器内有足量的Na2O2固体),此时容器的压强为p1,用电火花不间断的点燃,使其充分反应,恢复至原温,结果固体增重14g,此时容器的压强为p2,则p1/p2为()
| A.9:4 | B.7:3 | C.7:6 | D.6:7 |
将50g钠和铝的混合物投入到足量的水里,充分反应后,溶液中无固体剩余,则得到氢气的物质的量可能是 ( )
| A.0.8mol | B.1.8mol | C.2.2mol | D.0mol |