控制适合的条件,将反应2Fe3++2I- 2Fe2++I2设计成如右图所示的原电池(盐桥起到导电作用)。下列判断不正确的是
2Fe2++I2设计成如右图所示的原电池(盐桥起到导电作用)。下列判断不正确的是
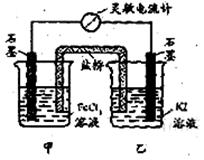

A.反应开始时,乙中石墨电极上发生氧化反应 |
B.反应开始时,甲中石墨电极作负极 |
C.电流计读数为零时,反应达到化学平衡状态 |
D.电流计读数为零后,在甲中溶入FeCl2,电流表可能会再次产生偏转 |
关于碱金属单质的性质叙述错误的是()
| A.在空气中燃烧都能生成过氧化物 | B.都能够与水反应 |
| C.都有较强的还原性 | D.最高价氧化物对应水化物都是强碱 |
元素的种类与原子的种类()
| A.前者大 | B.相同 | C.后者大 | D.无法确定 |
已知115号元素原子有七个电子层,且最外层有5个电子,试判断115号元素在元素周期表中的位置是()
| A.第七周期第IIIA族 | B.第七周期第VA族 |
| C.第七周期第IIIB族 | D.第七周期第VB族 |
113号元素原子(质量数是284)的中子数与质子数之差是()
| A.58 | B.0 | C.171 | D.60 |
放射性同位素钬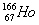 的原子核内的中子数与核外电子数之差是()
的原子核内的中子数与核外电子数之差是()
| A.99 | B.67 | C.32 | D.166 |