A、B、C、D、E、F、X七种物质之间可按下列框图发生反应(部分产物可能被省略)。其中,A、D、E、X是四种常见的非金属单质,常温下A、X为气体,D、E为固体。A的水溶液具有漂白性,A、D的水溶液均能使淀粉KI试纸变蓝色,B的焰色反应为黄色。请回答下列问题:
(1)写出A、F的化学式:A: 、F: 。
(2)写出B的电子式: ,EO2的晶体类型为 。
(3)写出E与NaOH溶液反应的离子方程式 。
(4)E单质可作高能燃料。已知ag固体E燃烧放出bkJ的热量,请写出表示E燃烧热的热化学方程式(△H用含a、b的式子表示) 。
硫酸是一种重要的基本化工产品。接触法制硫酸生产中的关键工序是SO 2的催化氧化:SO 2(g) O 2(g) SO 3(g)△H=﹣98kJ•mol ﹣ 1.回答下列问题:
(1)钒催化剂参与反应的能量变化如图(a)所示,V 2O 5(s)与SO 2(g)反应生成VOSO 4(s)和V 2O 4(s)的热化学方程式为: 。

(2)当SO 2(g)、O 2(g)和N 2(g)起始的物质的量分数分别为7.5%、10.5%和82%时,在0.5MPa、2.5MPa和5.0MPa压强下,SO 2平衡转化率α随温度的变化如图(b)所示。反应在5.0MPa、550℃时的α= ,判断的依据是 。影响α的因素有 。
(3)将组成(物质的量分数)为2m% SO 2(g)、m% O 2(g)和q% N 2(g)的气体通入反应器,在温度t、压强p条件下进行反应。平衡时,若SO 2转化率为α,则SO 3压强为 ,平衡常数K p= (以分压表示,分压=总压×物质的量分数)。
(4)研究表明,SO 2催化氧化的反应速率方程为:v=k( 1) 0.8(1﹣nα′)式中:k为反应速率常数,随温度t升高而增大;α为SO 2平衡转化率,α′为某时刻SO 2转化率,n为常数。在α′=0.90时,将一系列温度下的k、α值代入上述速率方程,得到v~t曲线,如图(c)所示。

曲线上v最大值所对应温度称为该α′下反应的最适宜温度t m.t<t m时,v逐渐提高;t>t m后,v逐渐下降。原因是 。
为验证不同化合价铁的氧化还原能力,利用下列电池装置进行实验。
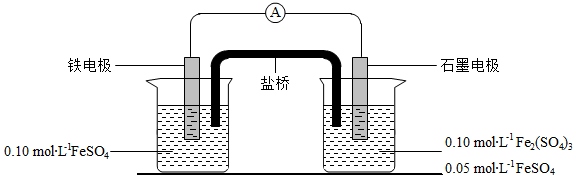
回答下列问题:
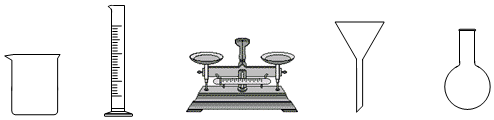
(1)由FeSO 4•7H 2O固体配制0.10mol•L ﹣ 1FeSO 4溶液,需要的仪器有药匙、玻璃棒、 (从下列图中选择,写出名称)。
(2)电池装置中,盐桥连接两电极电解质溶液。盐桥中阴、阳离子不与溶液中的物质发生化学反应,并且电迁移率(u ∞)应尽可能地相近。根据下表数据,盐桥中应选择 作为电解质。
|
阳离子 |
u ∞×10 8/(m 2•s ﹣ 1•V ﹣ 1) |
阴离子 |
u ∞×10 8/(m 2•s ﹣ 1•V ﹣ 1) |
|
Li + |
4.07 |
HCO 3 ﹣ |
4.61 |
|
Na + |
5.19 |
NO 3 ﹣ |
7.40 |
|
Ca 2+ |
6.59 |
Cl ﹣ |
7.91 |
|
K + |
7.62 |
SO 4 2 ﹣ |
8.27 |
(3)电流表显示电子由铁电极流向石墨电极。可知,盐桥中的阳离子进入 电极溶液中。
(4)电池反应一段时间后,测得铁电极溶液中c(Fe 2+)增加了0.02mol•L ﹣ 1.石墨电极上未见Fe析出。可知,石墨电极溶液中c(Fe 2+)= 。
(5)根据(3)、(4)实验结果,可知石墨电极的电极反应式为 ,铁电极反应式为 。因此,验证了Fe 2+氧化性小于 ,还原性小于 。
(6)实验前需要对铁电极表面活化。在FeSO 4溶液中加入几滴Fe 2(SO 4) 3溶液,将铁电极浸泡一段时间,铁电极表面被刻蚀活化。检验活化反应完成的方法是 。
羟基乙酸钠易溶于热水,微溶于冷水,不溶于醇、醚等有机溶剂。制备少量羟基乙酸钠的反应为ClCH2COOH+2NaOH→HOCH2COONa+NaCl+H2O△H<0
实验步骤如下:
步骤1:在如图所示装置的反应瓶中,加入40g氯乙酸、50mL水,搅拌。逐步加入40% NaOH溶液,在95℃继续搅拌反应2小时,反应过程中控制pH约为9。
步骤2:蒸出部分水至液面有薄膜,加少量热水,趁热过滤。滤液冷却至15℃,过滤得粗产品。
步骤3:粗产品溶解于适量热水中,加活性炭脱色,分离掉活性炭。
步骤4:将去除活性炭后的溶液加到适量乙醇中,冷却至15℃以下,结晶、过滤、干燥,得羟基乙酸钠。
(1)步骤1中,如图所示的装置中仪器A的名称是 ;逐步加入NaOH溶液的目的是 。
(2)步骤2中,蒸馏烧瓶中加入沸石或碎瓷片的目的是 。
(3)步骤3中,粗产品溶解于过量水会导致产率 ( 填“增大”或“减小”);去除活性炭的操作名称是 。
(4)步骤4中,将去除活性炭后的溶液加到适量乙醇中的目的是 。

以铁、硫酸、柠檬酸、双氧水、氨水等为原料可制备柠檬酸铁铵[(NH4)3Fe(C6H5O7)2].
(1)Fe基态核外电子排布式为 ;[Fe(H2O)6]2+中与Fe2+配位的原子是 (填元素符号).
(2)NH3分子中氮原子的轨道杂化类型是 ;C、N、O元素的第一电离能由大到小的顺序为 .
(3)与NH4+互为等电子体的一种分子为 (填化学式).
(4)柠檬酸的结构简式如图.1mol柠檬酸分子中碳原子与氧原子形成的σ键的数目为 mol.

CO2/HCOOH循环在氢能的贮存/释放、燃料电池等方面具有重要应用。
(1)CO2催化加氢。在密闭容器中,向含有催化剂的KHCO3溶液(CO2与KOH溶液反应制得)中通入H2生成HCOO﹣,其离子方程式为 ;其他条件不变,HCO3﹣转化为HCOO﹣的转化率随温度的变化如图1所示。反应温度在40℃~80℃范围内,HCO3﹣催化加氢的转化率迅速上升,其主要原因是 。

(2)HCOOH燃料电池。研究HCOOH燃料电池性能的装置如图2所示,两电极区间用允许K+、H+通过的半透膜隔开。
①电池负极电极反应式为 ;放电过程中需补充的物质A为 (填化学式)。
②如图2所示的HCOOH燃料电池放电的本质是通过HCOOH与O2的反应,将化学能转化为电能,其反应的离子方程式为 。
(3)HCOOH催化释氢。在催化剂作用下,HCOOH分解生成CO2和H2可能的反应机理如图3所示。
①HCOOD催化释氢反应除生成CO2外,还生成 (填化学式)。
②研究发现:其他条件不变时,以HCOOK溶液代替HCOOH催化释氢的效果更佳,其具体优点是 。