芳香族有机物A(C11H12O2)可用作果味香精。用含碳、氢、氧三种元素的有机物B和C为原料可合成A。请按所给信息及相关要求填空:
(1)有机物B的蒸气密度是同温同压下氢气密度的23倍,分子中碳、氢原子个数比为1:3。有机物B的分子式为 。
(2)有机物C的分子式为C7H8O,C能与钠反应,不与碱反应,也不能使溴的四氯化碳溶液褪色。C的名称为 。
(3)已知两个醛分子间能发生如下反应(﹣R、﹣R′表示氢原子或烃基):
用B和C为原料按如下路线合成A: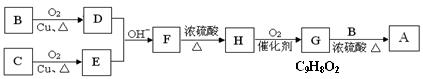
①上述合成过程中涉及的反应类型有: (填写序号)
a.取代反应 b. 加成反应 c. 消去反应 d. 氧化反应 e. 还原反应
② F的结构简式为: 。
③G和B反应生成A的化学方程式: 。
(4)F的同分异构体有 多种,写出既能发生银镜反应又能发生水解反应,且苯环上只有一个取代基的所有同分异构体的结构简式 。
多种,写出既能发生银镜反应又能发生水解反应,且苯环上只有一个取代基的所有同分异构体的结构简式 。
某化学实验小组拟用50mLNaOH溶液吸收CO2气体(用大理石和稀盐酸反应来制取CO2),以制备纯净的Na2CO3溶液。为了防止通入的CO2气体过量生成NaHCO3,他们设计了如下实验过程:
a.取25 mL NaOH溶液,向其中通入过量的CO2气体,至CO2气体不再溶解;
b.小火煮沸此溶液1~2 min;
c.在得到的溶液中加入另一半(25mL)NaOH溶液,使其充分混合反应。
(1)此方案能制得较纯净的Na2CO3,写出a、c两步的化学反应方程式:____________________________________、_____________________________________
(2)煮沸溶液的目的是。
此方案第一步的实验装置如右图所示: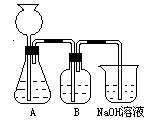
(3)加入反应物前,如何检查整个装置的气密性_________________________________。
(4)装置B中盛放的试剂是____________,作用是__________________________________。
(5)在实验室制法中,装置A还可作为下列_____________气体的发生装置(填序号)。
①CH2=CH2②H2S③CH4④CH≡CH⑤H2
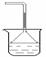
(6)实验室制取下列气体:①NH3,②Cl2,③HCl,④H2S,⑤CH4,⑥CO,⑦CO2,⑧O2时,属于必须进行尾气处理并能用下图所示装置进行处理的,将气体的序号填入装置图的下方空格内。
| 尾 气 吸 收 装 置 |
 |
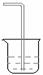 |
| 处理气体 |
(7)已知所用NaOH溶液中溶质的质量分数为40%,室温下该溶液密度为1.44 g / mL,假设反应前后溶液的体积不变,不考虑实验误差,计算用此种方法制备所得Na2CO3溶液的物质的量浓度为_________________。
用图1所示的Ⅰ和Ⅱ装置组合与Ⅰ和Ⅲ装置组合可以进行相关实验(夹持仪器省略),回答下列问题:
(1)若用Ⅰ和Ⅱ装置或Ⅰ和Ⅲ装置组合,实验前须检验。
(2)在Ⅰ和Ⅱ装置组合中,若a为浓硫酸,b为铜粉,c容器中盛放品红溶液,旋开f后,给烧瓶加热,一段时间后c中的现象是写出烧瓶中发生反应的化学方程式
(3)在Ⅰ装置中,若a为浓氨水,b为生石灰,欲制取氨气并证明氨水有碱性,最好应选用(填“Ⅱ”或“Ⅲ”)装置与其组合,原因是
(4)在Ⅰ装置中,若a为可能含有Mg2+、Cu2+、Al3+、Fe3+四种阳离子的水溶液,b为过氧化钠固体,旋开f后,有白色沉淀产生并放出氧气,过氧化钠固体的物质的量与产生沉淀的质量关系如图2,则a溶液中含有的阳离子有 。(写化学式)
(5)在图2中A→B段反应过程中溶液所增加的阴离子是(写化学式)
某实验小组用下列装置进行乙醇催化氧化的实验。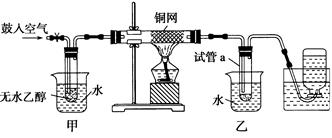
(1)实验过程中铜网出现红色和黑色交替的现象,请写出相应的化学反应方程式
___________________ ____________________________________________________.
在不断鼓入空气的情况下,熄灭酒精灯,反应仍能继续进行,说明该乙醇氧化反应
是________反应。
(2)甲和乙两个水浴作用不相同。甲的作用是________;乙的作用是________。
(3)反应进行一段时间后,干燥试管a中能收集到不同的物质,它们是_________________。集气瓶中收集到的气体的主要成分是____________。
(4)若试管a中收集到的液体用紫色石蕊试纸检验,试纸显红色,说明液体中还含有
________。要除去该物质,可先在混合液中加入________(填字母序号)。
a.氯化钠溶液b.苯 c.碳酸氢钠溶液 d.四氯化碳
然后,再通过________(填实验操作名称)即可除去。
实验室用乙酸和正丁醇制备乙酸正丁酯的原理如下:
CH3COOH+CH3CH2CH2CH2OH  CH3COOCH2CH2CH2CH3+H2O
CH3COOCH2CH2CH2CH3+H2O
有关物质的物理性质如下表,请回答有关问题。
| 化合物 |
密度/g·cm-3 |
沸点/℃ |
溶解度/g |
| 正丁醇 |
0.810 |
118.0 |
9 |
| 冰醋酸 |
1.049 |
118.1 |
∞ |
| 乙酸正丁酯 |
0.882 |
126.1 |
0.7 |
Ⅰ.乙酸正丁酯粗产品的制备
在干燥的50 mL圆底烧瓶中,装入沸石,加入11.5 mL正丁醇和9.4 mL冰醋酸,再加3~4滴浓硫酸,然后安装分水器(作用:实验过程中不断分离除去反应生成的水)、温度计及冷凝回流管,加热冷凝回流反应。
(1)沸石的作用
________________________________________________________________________。
(2)实验中为了提高乙酸正丁酯的产率,采取的措施是
______________________________;
________________________________________________________________________。
Ⅱ.乙酸正丁酯粗产品精制
(3)将乙酸正丁酯粗产品用如下的操作进行精制:①水洗 ②蒸馏 ③用无水MgSO4干燥 ④用10%碳酸钠溶液洗涤。正确的操作步骤是________(填字母)。
A.①②③④ B.③①④② C.①④①③② D.④①③②③
聚合硫酸铁又称聚铁,化学式为[Fe2(OH)n(SO4)3-0.5n]m,广泛用于污水处理。实验室利用硫酸厂烧渣(主要成分为铁的氧化物及少量FeS、SiO2等)制备聚铁和绿矾(FeSO4·7H2O),过程如下: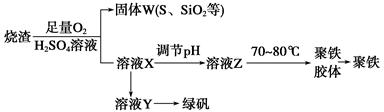
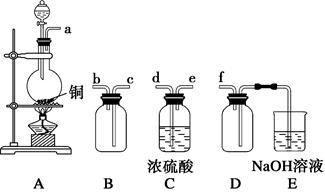
(1)验证固体W焙烧后产生的气体含有SO2的方法是________________。
(2)实验室制备、收集干燥的SO2,所需仪器如下。装置A产生SO2,按气流方向连接各仪器接口,顺序为a→________→________→________→________→f。
装置A中发生反应的化学方程式为___________________。
(3)制备绿矾时,向溶液X中加入过量________,充分反应后,经过滤操作得到溶液Y,再经浓缩、结晶等步骤得到绿矾。过滤所需的玻璃仪器有________________。
(4)欲测定溶液Y中Fe2+的浓度,需要用容量瓶配制KMnO4标准溶液,用KMnO4标准溶液滴定时应选用________滴定管(填“酸式”或“碱式”)。
(5)溶液Z的pH影响聚铁中铁的质量分数。若溶液Z的pH偏小,将导致聚铁中铁的质量分数________(填“偏大”、“偏小”或“无影响”)。