请回答下面问题
(1)Mg是第三周期元素,该周期部分元素氟化物的熔点见下表:
| 氟化物 |
NaF |
MgF2 |
SiF4 |
| 熔点/K |
1266 |
1534 |
183 |
解释表中氟化物熔点差异的原因:
。
(2)CO的结构可表示为C≡O,N2的结构可表示为N≡N。下表是两者的键能数据:(单位:kJ·mol-1)
| |
C-O |
C=O |
C≡O |
| CO |
357.7 |
798.9 |
1071.9 |
| |
N-N |
N=N |
N≡N |
| N2 |
154.8 |
418.4 |
941.7 |
CO与N2的结构相似,分子中都含有共价三键,其中含有 个π键;结合数据说明CO比N2活泼的原因:
。
(每空1分,共8分)
由丙烯经下列反应可得到F和高分子化合物G,它们都是常用的塑料
请回答下列问题:
(1)F的同分异构体有很多,其中属于芳香烃(除去F自身外)有种,化合物E的官能团的名称:、。
(2)写出下列反应过程的反应类型:A→B:、E→G。
(3)写出B→C反应的化学方程式为。
(4)若A在NaOH的醇溶液反应,生成物仍为卤代烃,且其结构存在顺反异构,那么,A所发生的反应的化学方程式为。
(5)E的一种同分异构体M具有如下性质:①能发生银镜反应;②1mol M与足量的金属钠反应可产生1mol H2,则M的结构简式为_________ ____。(注:两个羟基连在同一碳上的结构不稳定)
(每空2分,共14分)A、B、C、D均为含苯环的化合物,且相对分子质量B>A>C,已知有机物A的结构简式为:
(1)A既能和NaOH溶液反应,又能和NaHCO3溶液反应,写出A和 NaHCO3溶液反应的化学方程式________________。
(2)①有机物B在浓硫酸存在条件下,相互作用生成一种环状酯(如下图)则有机物B的结构简式为_。
②等物质的量B与Na、NaOH、NaHCO3充分反应,消耗Na、NaOH、NaHCO3的物质的量之比为________。
(3) 1molA、C完全燃烧,消耗O2的质量相等,且1molC能和1molNa完全反应,写出含碳原子数最少的C的结构简式________,写出C与浓溴水的反应的化学方程式。
(4)D和B互为同分异构体,且知其苯环上连有三个取代基,苯环上的一氯代物只有两种,D不与NaHCO3溶液反应,能与Na和NaOH反应,等质量的D消耗Na和NaOH的物质的量之比为2∶3,则D的结构简式为、。(只写二种)
(每空2分,共8分)分子式为C3H6O3的物质有多种同分异构体,请写出符合下列要求的各种同分异构体的结构简式:(均用结构简式完成)
(1)A能与NaHCO3溶液反应,且1 molA与足量金属Na能生成1 molH2,则
A为或。
(2)B中所有同类原子的化学环境等同(如CH4中所有H所处化学环境等同),且不与Na反应,则B为。
(3)C中碳与氧分别有两种化学环境,氢的环境等同,且C与Na不反应,则C为。
(8分)X、Y、Z、W为按原子序数由小到大排列的四种短周期元素。
已知:①X可分别与Y、W形成X2Y、X2Y2、XW等共价化合物;②Z可分别与Y、W形成Z2Y、Z2Y2、ZW等离子化合物。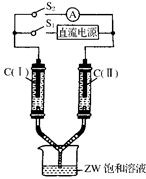
请回答:
(1)Z2Y的化学式是________________________。
(2)Z2Y2与X2Y反应的化学方程式是_______________________________________
(3)如图所示装置,两玻璃管中盛满滴有酚酞溶液的ZW饱和溶液,C(Ⅰ)、C(Ⅱ)为多孔石墨电极。接通S1后,C(Ⅰ)附近溶液变红,两玻璃管中有气体生成。一段时间后(两玻璃管中液面未脱离电极),断开S1,接通S2,电流表的指针发生偏转。此时:
C(Ⅰ)的电极名称是________(填写“正极”或“负极”);
C(Ⅱ)的电极反应式是________________________________。
(4)铜屑放入稀硫酸不发生反应,若在稀硫酸中加入X2Y2,铜屑可逐渐溶解,该反应的离子方程式是____________________________________。
根据下列五种元素的电离能数据(单位:kJ/mol),回答下面各题。
| 元素代号 |
I1 |
I2 |
I3 |
I4 |
| Q |
2080 |
4000 |
6100 |
9400 |
| R |
500 |
4600 |
6900 |
9500 |
| S |
740 |
1500 |
7700 |
10500 |
| T |
580 |
1800 |
2700 |
11600 |
| U |
420 |
3100 |
4400 |
5900 |
(1)在周期表中,最可能处于同一族的是()
A.Q和R B.S和T C.T和U D.R和T E.R和U
(2)电解它们的熔融氯化物,阴极放电反应最可能正确的是()
A.Q2++2e-→Q B.R2++2e-→R
C.S3++3e-→SD.T3++3e-→TE.U2++2e-→U
(3)它们的氯化物的化学式,最可能正确的是()
A.QCl2 B.RCl C.SCl3 D.TCl E.UCl4
(4)S元素最可能是()
A.S区元素 B.稀有气体元素 C.p区元素D.准金属E.d区元素
(5)下列元素中,化学性质和物理性质最像Q元素的是()
A.硼(1s22s22p1) B.铍(1s22s2) C.锂(1s22s1)D.氢(1s1) E.氦(1s2)