【化学-物质结构与性质】
利用有关知识回答下列问题:
(1)B、F两元素形成的化合物的空间构型为 ,其中心原子的杂化类型为 。
(2)CH4与 (写微粒符号)互为等电子体。
(3)写出元素Cu基态原子的电子排布式 。
(4)Fe与CO可形成的Fe(CO)5型化合物,该化合物常温下呈液态,熔点为-20.5℃,沸点为103℃,易溶于非极性溶剂,据此可判断该化合物晶体属于 晶体(填晶体类型)。
(5)Zn的离子的氢氧化物不溶于水,但可溶于氨水中,该离子与NH3间结合的作用力为 。
(6)金属Fe的晶体在不同温度下有两种堆积方式,晶胞分别如右图所示。则面心立方晶胞和体心立方晶胞中实际含有的原子个数之比为 。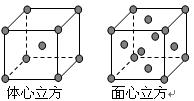
、A、B、C、D为三种不同的配合物,它们的化学式都是CrCl3·6H2O,但颜色不同: A呈亮绿色,13.325g跟足量AgNO3溶液反应,得到了14.35沉淀;B呈暗绿色,能沉淀1/3的氯;而C呈紫色,可沉淀出全部氯元素;D的溶液跟足量AgNO3溶液不反应,将D在一定温度下,加热分解测得质量减少20.26%。
(1)则它们的结构简式分别为:
A,B,C, D。
2)请画出A结构图。
四种短周期元素的性质或结构信息如下表。请根据信息回答下列问题。
| 元素 |
A |
B |
C |
D |
| 性质 结构 信息 |
室温下单质呈粉末状固体,加热易熔化。单质在空气中燃烧,发出明亮的蓝紫色火焰。 |
单质常温、常压下是气体,能溶于水。原子的M层有1个未成对的p电子。 |
单质质软、银白色固体、导电性强。单质在空气中燃烧发出黄色的火焰 。 。 |
原子最外电子层上s电子数等于p电子数,等于电子层数。 |
(1)B元素在周期表中的位置是___区,写出A离子的电子排布式___
(2)写出C单质与水反应的离子方程式________
(3)A、B、C、D四种元素的第一电离能由大到小的顺序________
(4)A、B两元素非金属性较强的是(写元素符号)________。写出证明这一结论的一个
实验事实________
(10分)X、Y、Z、W是元素周期表前四周 期中的四种常见元素,其相关信息如下表:
期中的四种常见元素,其相关信息如下表:
| 元素 |
相关信息 |
| X |
X的基态原子核外3个能级上有电子,且每个能级上的电子数相等 |
| Y |
Y元素的激发态原子的电子排布式为1s22s22p63s23p34s1 |
| Z |
Z和Y同周期,Z的电负性大于Y |
| W |
W的一种核素的质量数为63, 中子数为 中子数为 34 34 |
(1)Y元素基态原子的电子排布式为。
(2)Y的简单离子半径Z的简单离子半径(选填“>”、“=”、“<”)。
(3)XY2是一种常用的溶剂,XY2的分子中存在 个σ键。在H―Y、H―Z两种共价键中,键的极性较强的是 ,键长较长的是 。
(4)向WYO4的水溶液中逐滴加入氨水至过量,观察到现象为 。反应过程中涉及的离子方程式为:、
。反应过程中涉及的离子方程式为:、
。
(11分)下表为长式周期表的一部分,其中的编号代表对应的元素。
| ① |
|||||||||||||||||
| ② |
③ |
||||||||||||||||
| ④ |
⑤ |
⑥ |
⑦ |
||||||||||||||
| ⑧ |
 |
⑨ |
请回答下列问题:
(1)表中元素①的6个原子与元素③的6个原子形成的某种环状分子名称为;③和⑦形成的一种常见溶剂的化学式为,其立体构型为________________。
(2)某元素原子的外围电子排布式为nsnnpn+1,该元素原子的最外电子层上孤电子对数为;该元素与元素①形成的最简单分子X属于分子(填“极性”或“非极性”)。
(3)元素④的第一电离能元素⑤(选填“>”、“=”、“<”)的第一电离能;元素⑥的电负性元素⑦(选填“>”、“=”、“<”)的电负性。
(4)元素⑦和⑧形成的化合物的电子式为 。
。
(5)元素⑨的基态原子核外电子排布式是 。
(6)某些不同族元素的性质也有一定的相似性,如上表中元素②与元素⑤的氢氧化物有相似的性质。请写出元素②的氢氧化物与NaOH溶液反应的化学方程式:
__________________________________________________________________________
、有A、B、C、D四种元素。已知A的单质是同温同压下的气体中密度最小的;B的原子中电子只填充在两种轨道上,还有一个空轨道;C原子基态中能量最高的能级电子排布为2p4,D的单质分子中有一个σ键,两个π键。A、D的原子序数之和与C相等。
(1)B在元素周期表中的位置是。
(2)D的最外层电子排布是。
(3)A与B形成的原子数最少的分子的结构式为。
(4)A、B、C、D四元素能形成一种离子化合物,该化合物的化学式为。