、A、B、C、D为三种不同的配合物,它们的化学式都是CrCl3·6H2O,但颜色不同: A呈亮绿色,13.325g跟足量AgNO3溶液反应,得到了14.35沉淀;B呈暗绿色,能沉淀1/3的氯;而C呈紫色,可沉淀出全部氯元素;D的溶液跟足量AgNO3溶液不反应,将D在一定温度下,加热分解测得质量减少20.26%。
(1)则它们的结构简式分别为:
A ,B ,C , D 。
2)请画出A结构图。
(1)用油脂水解制取高级脂肪酸和甘油,通常选择的条件是________;若制取肥皂和甘油,则选择的条件是____________;液态油转化为固态脂肪通常在________________条件下,用油跟________反应。
(2)A、B两种溶液,一种是植物油,一种是矿物油。现各取少量,放在两只洁净的试管里,加入NaOH溶液并加热,冷却后加水振荡,A出现泡沫,B无明显现象。由此可推出:A为________,B为________;理由是___________________________。
某天然油脂A的分子式为C57H106O6。1摩尔该油脂水解可得到1摩尔甘油、1摩尔不饱和脂肪酸B和2摩尔直链饱和脂肪酸C。经测定B的相对分子质量为280,原子个数比为N(C)∶N(H)∶N(O)=9∶16∶1。
(1)写出B的分子式:_______________________________________。
(2)写出C的结构简式:____________;C的名称是______________。
(3)写出含5个碳原子的C的同系物的同分异构体的结构简式:__________________。
森林是国民经济的宝贵资源,它不仅提供木材和多种林副产品,而且在保护环境、维持生态平衡方面起着极为重要的作用,试回答:
(1)森林通过什么途径吸收CO2,防止温室效应?
_______________________________________________________________。
(2)木材是重要的化工原料,其主要成分是纤维素,纤维素分子由很多个________单元构成,在每个单元中含有________个羟基,所以纤维素能发生________反应,它与浓H2SO4和浓HNO3的混合物发生反应的化学方程式是____________________________________。
(3)纤维素在浓硫酸的作用下水解的最终产物是________________(填结构简
式)。写出在医学上检验该物质的化学方程式__________________。
如图所示,淀粉水解可产生某有机化合物A,A在不同的氧化剂作用下,可以生成B(C6H12O7)或C(C6H10O8),B和C都不能发生银境反应。A、B、C都可以被强还原剂还原成为D(C6H14O6)。B脱水可得五元环的酯类化合物E或六元环的酯类化合物F。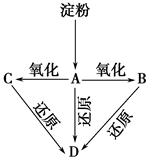
已知:相关物质被氧化的难易次序是:RCHO最易,R—CH2OH次之,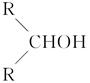 最难。
最难。
请在下列空格中填写A、B、C、D、E、F的结构简式。
A.____________________;B.____________________;
C.____________________;D.____________________;
E.____________________;F.____________________。
A、B、C是大家熟悉的与生命运动密切相关的三种化合物,它们所含元素不超过三种,并有下图所示的转化关系。其中化合物D也是日常生活中常见的化合物,在一定条件下可与单质X发生如下变化:D+3X―→3A+2B,回答下列有关问题: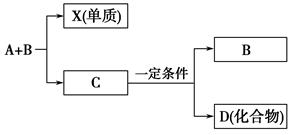
(1)在A、B、C、D四种化合物中,所含元素相同的是(写物质名
称)______________________。
(2)常温下,A和B是通过________________转化成C的,该转化的实质是_______________________________________________________________。
(3)目前,化合物B在自然界中的含量逐渐上升,它会引起_____________。
(4)写出D跟浓硫酸和乙酸共热时的反应方程式:_____________________。