(14分)
现有A、B、C、D、E、F六种短周期主族元素,它们的原子序数依次增大,D与E的氢化物分子构型都是V型.A、B原子的最外层电子数之和与C原子的最外层电子数相等,A能分别与B、C、D形成电子总数相等的分子,且A与D可形成的化合物常温下均为液态.请回答下列问题(填空时用实际物质的化学式表示):
(1)C与F两种元素形成一种化合物分子,各原子最外层达8电子结构,则该分子的结构式 ,其空间构型为 .
(2)科学家制出另一种直线型气态化合物 B2D2分子,且各原子最外层都满足8电子结构,则B2D2电子式为 .
(3)C4分子结构如题26图所示,已知断裂lmol C-C吸收167kJ热量,生成1mo1C≡C放出942kJ热量.则下列说法正确的是 .
① C4属于一种新型的化合物 ② C4沸点比P4(白磷)低
③ lmol C4气体转变为C2吸收882kJ热量 ④ C2与C4互为同素异形体
⑤ C4与C2互为同分异构体
(4)已知A2(g)与C2(g)一定条件下反应生成0.5mol CA3(g)放出23kJ的热量,写出该反应的热化学方程式 .
(5)为了除去化合物乙(A2ED4)的稀溶液中混有的A2ED3,常加入氧化剂A2D2,发生反应的离子方程式为: .
下列有关实验的叙述,正确的是 (填序号)
| A.分液时,分液漏斗下层液体从下口放出,上层液体从上端口倒出 |
| B.氢气还原氧化铜实验中,先加热氧化铜后通氢气 |
| C.蒸馏石油时,加热一段时间后发现未加碎瓷片,立刻拔开橡皮塞并投入碎瓷片 |
| D.实验室做钠的实验时,余下的钠屑投入到原试剂瓶中 |
E.浓硫酸不小心沾到皮肤上,立刻用稀NaOH溶液洗涤
F.不慎将苯酚沾到皮肤上,立即用酒精清洗;
G.配制浓硫酸和浓硝酸的混合酸时,将浓硫酸沿器壁慢慢加入浓硝酸中,并不断搅拌;
H.配制银氨溶液时,将稀氨水慢慢滴加到硝酸银溶液中,产生沉淀后继续滴加到沉淀刚好溶解为止
I.用浓盐酸清洗做过高锰酸钾分解实验的试管
J.存放氯化亚铁溶液的试剂瓶则加些铁粉和稀盐酸
K.在实验室中常用加热NH4Cl固体的方法来制取氨气。
研究证明:使用氯气作自来水消毒剂,氯气会与水中有机物反应,生成如CHCl3等物质,这些物质可能是潜在的致癌致畸物质,目前人们已研发多种饮用水的新型消毒剂。亚氯酸钠(NaClO2)常用于水的消毒和砂糖、油脂的漂白与杀菌。以下是用过氧化氢法生产亚氯酸钠的工艺流程图:
已知:①NaClO2的溶解度随温度升高而增大,适当条件下可结晶析出NaClO2·3H2O。
②纯ClO2易分解爆炸,一般用稀有气体或空气稀释到10%以下较安全;
(1)在发生器中鼓入空气的作用可能是_________________________________。吸收塔内发生反应的化学方程式为_____________________。该工艺流程中的NaClO3、ClO2、NaClO2都是强氧化剂,它们都能和浓盐酸反应制取Cl2。若用二氧化氯和浓盐酸制取Cl2,当生成0.5 mol Cl2时,反应中转移电子的个数是________。
(2)吸收塔的温度不能超过20℃,其目的是_____________。吸收塔中为防止NaClO2被还原成NaCl,所用还原剂的还原性物质中除H2O2外,还可以选择的还原剂是_____(选填序号)。
a.Na2O2 b.Na2S c.FeCl2
(3)从滤液中得到的NaClO2·3H2O晶体的操作依次是__________(填写序号)。
a.蒸发 b.灼烧 c.过滤 d.冷却结晶
(4)印染工业常用亚氯酸钠(NaClO2)漂白织物。亚氯酸钠(NaClO2)在溶液中可生成ClO2、HClO2、ClO2-、Cl-等,其中HClO2和ClO2都具有漂白作用,但ClO2是有毒气体,25℃时,各组分含量随pH变化情况如图所示(Cl-没有画出)。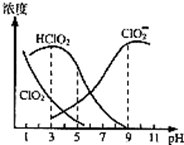
回答下列问题:
①该温度下NaClO2溶液中c(Na+)__________c(ClO2-)(填“>”“=”或“<”),原因是________________________________(用一个离子方程式表示);
②使用该漂白剂的最佳pH为_____;
| A.3.0 | B.4.0-4.5 | C.6.5-7.0 | D.9.0 |
③根据图中数据,当pH=8时,往NaClO2溶液中滴入稀盐酸,溶液中主要反应的离子方程式为_______。
请结合化学反应原理回答下列问题:
(1)硫酸的产量通常用来衡量一个国家的化学工业发展水平,硫酸工业生产中涉及反应之一为:
2SO2(g)+O2(g) 2SO3(g),SO2的平衡转化率与温度、压强的关系如右图所示。
2SO3(g),SO2的平衡转化率与温度、压强的关系如右图所示。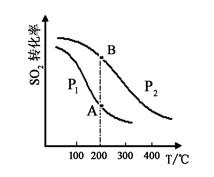
①压强:P1 P2(填“>”、“=”或“<”)。
②200℃下,将一定量的SO2和O2充入体积不变的密闭容器中,经10min后测得容器中各物质的物质的量浓度如下表所示:
| 气体 |
SO2 |
O2 |
SO3 |
| 浓度(mol/L) |
0.4 |
1.2 |
1.6 |
能说明该反应达到化学平衡状态的是 。
a.反应速率υ(SO2)=υ(SO3)
b.体系的压强保持不变
c.混合气体的密度保持不变
d.SO2和O2的体积比保持不变
计算上述反应在0~10min内,υ(SO2)= 。
(2)SO2与氢氧化钠溶液反应可以生成亚硫酸氢钠,已知25℃时,NaHSO3的水解平衡常数=1.0×10-12mol/L,则该温度下H2SO3 HSO3-+H+的电离常数Ka=____mol/L,若向H2SO3溶液中加入少量的I2,则溶液中
HSO3-+H+的电离常数Ka=____mol/L,若向H2SO3溶液中加入少量的I2,则溶液中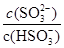 将________(填“增大”、“减小”或“不变”)。
将________(填“增大”、“减小”或“不变”)。
(3)工业制取硫酸还可以利用电化学原理:
①工业生产中用SO2为原料制取硫酸可以利用原电池原理,用SO2、O2和H2O来制备硫酸,该电池用多孔材料作电极,它能吸附气体,同时也能使气体与电解质溶液充分接触。请写出该电池的正极电极反应式_____________。
②用Na2SO3溶液充分吸收SO2得NaHSO3溶液,然后电解该溶液可制得硫酸。电解原理示意图如下图所示。请写出开始时阳极反应的电极反应式_________。
有A、B、C、D、E五种前四周期元素,原子序数依次增大,A元素一种同位素常用于文物年代测定,C元素的单质之一为淡蓝色气体,可阻挡对人体有害的紫外线,D为前四周期元素中电负性最小的元素,E原子核外最外层电子数与D相同,其余各层均充满。请根据以上信息,回答下列问题:
(1)A、B、C三种原子的第一电离能由大到小的顺序为______(用元素符号表示)。
(2)基态E+离子的核外电子排布式是 ,E的高价离子与B的最常见氢化物形成的配离子的化学式为 。
(3)化合物B2C与A元素的最高价氧化物互为等电子体,则化合物B2C的立体构型是 。
(4)化合物甲由C、D两种元素组成,其晶胞如甲图,甲的化学式___________。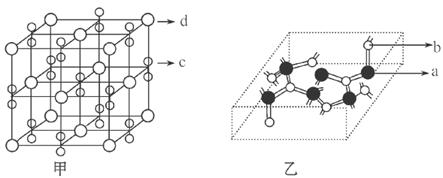
(5)化合物乙的部分结构如乙图,乙由A、B两元素组成,硬度超过金刚石。
①乙的晶体类型为________,其硬度超过金刚石的原因是______________。
②乙的晶体中A、B两种元素原子的杂化方式均为___________________。
为验证氧化性:Cl2>Fe3+>SO2,某小组用下图所示装置进行实验(夹持仪器和A中的加热装置已略,气密性已经检验完毕)
实验过程:
Ⅰ.打开弹簧夹K1-K4,通入一段时间N2,再将T型导管插入B中,继续通入N2,单后关闭K1、K2、K3 .
Ⅱ.打开活塞a,滴加一定量的浓盐酸,给A加热.
Ⅲ.当B中的溶液变黄时,停止加热,夹紧弹簧夹K2.
Ⅳ.打开活塞b,使约2ml的溶液流入D试管中,检验其中的离子.
Ⅴ.打开弹簧夹K3、活塞c,加入70%的硫酸,一段时间后夹紧弹簧夹K3.
Ⅵ.更新试管D,重复过程Ⅵ,检验B溶液中的离子.
(1)过程Ⅰ的目的是___________________________
(2)棉花中浸润的溶液为_______________________
(3)A中发生反应的化学方程式为_____________________________________________
(4)用70%的硫酸制取SO2,反应速率比用98%的硫酸快,原因是___________________
(5)过程Ⅳ中检验B溶液中是否含有硫酸根的操作是______________________________
(6)甲、乙、丙三位同学分别完成了上述实验,他们的检测结果一定能够证明氧化Cl2>Fe3+>SO2的是
| 过程Ⅳ B溶液中含有的离子 |
过程Ⅵ B溶液中含有的离子 |
|
| 甲 |
有Fe3+无Fe2+ |
有SO42- |
| 乙 |
既有Fe3+又有Fe2+ |
有SO42- |
| 丙 |
有Fe3+无Fe2+ |
有Fe2+ |