有关元素X、Y、Z、W的信息如下
| 元素 |
有关信息 |
| X |
所在主族序数与所在周期序数之差为4 |
| Y |
最高价氧化物对应的水化物,能电离出电子数相等的阴、阳离子 |
| Z |
单质是生活中常见金属,其制品在潮湿空气中易被腐蚀或损坏 |
| W |
地壳中含量最高的金属元素 |
请回答下列问题:
(1)W的单质与Y的最高价氧化物对应的水化物反应的离子方程式为 。
铜片、碳棒和ZX3溶液组成原电池,写出正极发生的电极反应方程式
_______________________________________________。
(2)向淀粉碘化钾溶液中滴加几滴ZX3的浓溶液,现象为_____________________,相关反应的离子方程式为_______________________________。
(3)以上述所得WX3溶液为原料制取无水WX3,先制得WX3·6H2O晶体,主要操作包括__________________________,在_____________________条件下加热WX3·6H2O晶体,能进(4)一步制取无水WX3,其原因是(结合离子方程式简要说明)_______________________________。
短周期元素 X、Y、Z 可组成化学式均为 XYZ3的四种化合物甲、乙、丙、丁。
(l)若甲中 X 的原子只有一个质子,Y 、Z均是第二周期元素,则 Y 元素原子的电子排布式为; X、Y 原子间可形成与烷烃结构类似的化合物,则该系列化合物的通式为。
(2)若乙是一种微溶于水的物质,其 Ksp 约为 6.8×10ˉ6,且 X、Y、Z 三种元素的原子序数之和为 26 , Y、Z 同周期,则乙的溶解平衡可表示为,其饱和溶液中X的离子的物质的量浓度约为mol/ L.
(3)若丙中X元素的焰色反应为黄色,Y与X同周期,Y 是同周期中原子半径最小的元素,丙与浓盐酸反应生成 Y 单质的化学方程式为.
(4)若丁中 X、Y、Z 处于不同周期,且 X 原子最外层电子数为其次外层电子数的二倍,Z原子最外层电子数是其电子层数的二倍多1,则丁的结构式为。
(12 分)能源问题是人类社会面临的重大课题。甲醇是未来重要的绿色能源之一。
(l)已知:在 25 ℃、101 kPa 下,1g 甲醇燃烧生成 CO2和液态水时放热 22.70kJ 。请写出甲醇燃烧的热化学方程式。
(2)由CO2和H2合成甲醇的化学方程式为:CO2(g)+ 3H2 (g)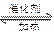 CH3OH(g)+H2O (g ).在其它
CH3OH(g)+H2O (g ).在其它 条件不变的情况下,实验测得温度对反应的影响如下图所示(注:T1、T2均大于300 ℃)
条件不变的情况下,实验测得温度对反应的影响如下图所示(注:T1、T2均大于300 ℃)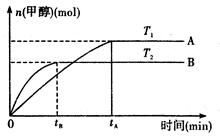
①合成甲醇反应的△H0。(填“>”、“<”或“=”)。
②平衡常数的表达式为:.温度为T2时的平衡常数温度为T1时的平衡常数(填“>”、“<”或“=”)
③在T1温度下,将1mol CO2和 1 molH2充入一密闭恒容容器中,充分反应达到平衡后,若CO2转化率为α,则容器内的压强与起始压强的比值为。
(3)利用甲醇燃料电池设计如下图所示的装置。
该装置中 Pt 极为极;写出 b极的电极反应式.
铁单质及其化合物在生活、生产中有广泛应用。请回答下列问题:
(1)黄铁矿(FeS2)是生产硫酸和冶炼钢铁的重要原料。其中一个反应为:3FeS2+8O2 6SO2+Fe3O4,3 mol FeS2参加反应转移mol电子。
6SO2+Fe3O4,3 mol FeS2参加反应转移mol电子。
(2)氯化铁溶液常用作印刷电路铜板腐蚀剂,反应的离子方程式。
从腐蚀废液回收得到金属铜还需要的试剂为_________________________。
(3)与明矾相似,硫酸铁也可用作絮凝剂,在使用时发现硫酸铁并不能使酸性废水中的悬浮物沉降除去,其原因是。
(4)下表中,对陈述I、II的正确性及其有无因果关系的判断都正确的是____。(填字母)
| 选项 |
陈述I |
陈述II |
判断 |
| A |
铁是地壳中含量最高的金属元素 |
铁是人类最早使用的金属材料 |
I对;II对;有 |
| B |
常温下铁与稀硫酸反应生成氢气 |
高温下氢气能还原氧化铁生成铁 |
I对;II对;无 |
| C |
铁属于过渡金属元素 |
铁和铁的某些化合物可以用作催化剂 |
I错;II对;无 |
| D |
铁在空气中表面生成致密氧化膜 |
可用铁罐储存运输浓硫酸、浓硝酸 |
I对;II对;有 |
有机物A1和A2分别和浓H2SO4在一定温度下共热都只生成烃B,B的蒸气密度是同温同压下H2密度的59倍,在催化剂存在下,1mol B可以和4mol H2发生加成反应,B的一元硝化产物有三种(同种类型)。有关物质之间的转化关系如下:
(1)反应①属于反应,反应②属于反应
(2)写出A2物质的结构简式:A2
(3)书写化学方程式:
③④⑤
(4)化合物E有多种同分异构体,其中属于酯类且具有两个对位侧链的同分异构体有四种,分别写出它们的结构简式: ;;;。
;;;。
将标准状况下的NH3 700L溶于1L的水中,所得溶液的密度为0.90g/cm3,则所得氨水的物质 的量浓度为mol/L
的量浓度为mol/L