(16分)、据《中国制药》报道,化合物F是用于制备“非典”药品(盐酸祛炎痛)的中间产物,其合成路线为:

|
已知:一定条件(Ⅰ)RNH2+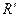 CH2Cl → RNHCH2
CH2Cl → RNHCH2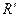 +HCl(R和
+HCl(R和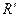 代表烃基);
代表烃基);
(Ⅱ)苯的同系物能被酸性高锰酸钾溶液氧化,如:
(Ⅲ) (苯胺,弱碱性,易氧化)
(苯胺,弱碱性,易氧化)
(Ⅳ)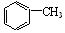 与浓硫酸、浓硝酸混合在不同温度下会得到不同产物
与浓硫酸、浓硝酸混合在不同温度下会得到不同产物
回答下列问题:
(1)C的结构简式是 。
(2)请写出D+E→F的化学方程式: 。
(3)E在一定条件下,可聚合成很好的功能高分子材料,写出合成此高聚物的化学方程式 。
(4)反应①~⑤中,属于取代反应的 是(填反应序号)
是(填反应序号)
(5)符合下列条件的E的同分异构体的数目是( )。
①与FeCl3溶液有显色反应 ②能发生银镜反应 ③苯环上的一溴取代物只有3种。
| A.3种 | B.8种 | C.10种 | D.12种 |
(6) 已知苯甲醛在一定条件下可以通过Perkin反应生成肉桂酸(产率45~50%),反应方程式如下:
C6H5CHO + (CH3CO)2O → C6H5CH="CHCOOH" +CH3COOH
苯甲醛 肉桂酸
若苯甲醛的苯环上有取代基,也能发生Perkin反应,相应产物的产率如下:
| 反应物 |
 |
|
|
|
| 产率(%) |
15 |
23 |
33 |
0 |
| 反应物 |
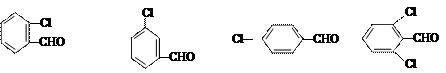 |
|
|
|
| 产率(%) |
71 |
63 |
52 |
82 |
请根据上表回答:取代基对Perkin反应的影响有(写出3条即可):
①
②
③ [来
(1)下图是一套实验室制气装置,用于发生、干燥和收集气体,下列各组物质中能利用这套装置进行实验的是_(填代号)。
①亚硫酸钠和硫酸②二氧化锰和浓盐酸③浓氨水和生石灰④石灰石和稀硫酸⑤锌和稀硫酸⑥硫化亚铁与稀硫酸⑦双氧水和二氧化锰
(2)有两瓶失去标签的物质的量浓度相同的碳酸钠溶液和碳酸氢钠溶液,请你加以鉴别:
①下列试剂中,可选用的一种试剂是_______(填代号)。
| A.氢氧化钠溶液 | B.甲基橙溶液 | C.稀盐酸 | D.澄清石灰水 |
②除上述方法外,你认为是否还有其它的方法,具体如何操作_______。
(3)实验室需要用纯净的NaCl溶液,现有的NaCl晶体中混有少量的Na2SO4和(NH4)2CO3,请设计实验除去杂质,并回答下列问题:
①除去(NH4)2CO3用加热好还是加强碱后再微热好?你选择的是,其理由是
。
②以下是除去SO42-的实验方案。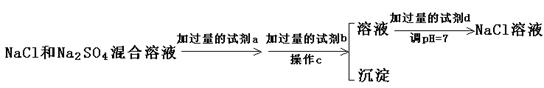
过量的a试剂是,C操作中所使用的玻璃仪器的名称是,证明SO42-已经沉淀完全的方法是 。
。
某同学取一定量淀粉进行水解实验,其实验步骤如下所示:
请回答下列问题:
①所加入的试剂分别是
A________,B________,C________;
②加B的原因是_____________________________________________________;
③由此可知淀粉是________(填“部分”、“完全”或“没有”)水解。
(10分)为回收和利用废旧塑料减轻“白色污染”,某兴趣小组进行如下探究:
<实验课题>废旧聚丙烯塑料热分解主要产物为烃的探究
<查阅资料>
①废旧聚丙烯塑料热分解的产物为常温下的气态烃和液态烃,且不含一氧化碳和氢气
②CuO能将烃氧化成CO2和H2O
③甲苯可被酸性KMnO4溶液氧化为苯甲酸,苯甲酸能溶于苯
<实验设计>
<实验记录>
①B装置试管中有液态物质生成;②C中溴水的颜色变浅;③E中黑色氧化铜变红;④F中无水硫酸铜变蓝。
<问题讨论>
请你参与实验设计的评价和实验结果的分析:
(1)经分析得知B装置试管中的液态产物是甲苯和苯的混合物。若要将两者分离,其实验方法是;若要除去混合物中的甲苯,其方法是向混合物中加入足量酸性KMnO4溶液,充分反应后,再加入一定量的NaOH溶液,充分反应,再。
(2)C装置的作用是;如果没有D装置,对实验结论产生的影响是。
(3)若需验证聚丙烯塑料热分解产物中确含气态烃,还需在F装置后增加一个实验装置,请将增加的装置图(要注明其中盛放的试剂名称)画在“实验设计”栏中的空白方框内。
海藻中含有丰富的碘元素(以I-形式存在)。实验室中提取碘的流程如下:
(1)实验操作③的名称是___________,所用主要仪器名称为______________________。
(2)提取碘的过程中,可选择的试剂是________________(已知碘的沸点为184.40C)。
A.酒精(沸点780C) B.四氯化碳(沸点770C)
C.甘油(沸点1900C) D.苯(沸点800C)
(3)操作②的离子方程式为;该步骤的含I2溶液中生成有少量ICl,为使碘全部以单质形式游离出来,应加入适量KI溶液,此反应的化学方程式为。
某探究小组用HNO3与大理石反应过程中质量减小的方法,研究影响反应速率的因素。所用HNO3浓度为1.00mol/L、2.00mol/L,大理石有细颗粒和粗颗粒两种规格,实验温度为25℃、35℃,每次实验HNO3的用量为25.00mL,大理石用量为10.00g。
(1)请完成以下实验设计表,并在实验目的一栏中填空:
| 实验 编号 |
温度 (℃) |
大理石 规格 |
HNO3浓度(mol/L) |
实验目的 |
| ① |
25 |
粗颗粒 |
2.00 |
(I)实验①和②探究浓度对反应速率的影响; (II)实验①和③探究温度对反应速率的影响; (III)实验①和④探究对反应速率的影响 |
| ② |
25 |
粗颗粒 |
||
| ③ |
粗颗粒 |
2.00 |
||
| ④ |
25 |
细颗粒 |
2.00 |
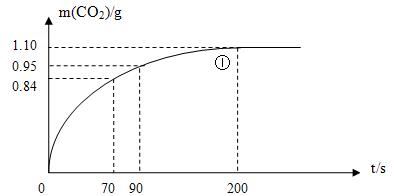
(2)实验①中CO2质量随时间变化的关系见下图。计算实验①中70s-90s范围内用HNO3/*-表示的平均反应速率(忽略溶液体积变化,不需要写出计算过程)。