由硫可制得多硫化钠Na2Sx,x的值一般为2~6。当x=2时,多硫化钠称为过硫化钠。
Ⅰ.过硫化钠加入盐酸中有硫沉淀析出,写出该反应的化学方程式 ,该反应的还原产物是 。
Ⅱ.某些多硫化钠可用于制作蓄电池。下图是一种正在投入生产的大型蓄电系统的原理图。电池中的左右两侧为电极,中间为离子选择性膜,在电池放电和充电时该膜只允许钠离子通过。电池充、放电的化学反应方程式为:


(1)电池中的左侧“电极”的电极名称是 (填“正极”或“负极”)。
(2)放电过程中钠离子从 (选“左到右”或“右到左”)通过离子交换膜。
(3)写出充电过程中阳极的电极反应式 。
一种以黄铜矿和硫磺为原料制取铜和其他产物的新工艺,原料的综合利用率较高。其主要流程如下: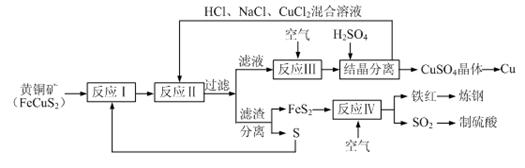
注:反应Ⅱ的离子方程式为Cu2++CuS+4Cl—=2CuCl2-+S
请回答下列问题:
⑴反应Ⅰ的产物为(填化学式) ▲。
⑵反应Ⅲ的离子方程式为 ▲。
⑶一定温度下,在反应Ⅲ所得的溶液中加入稀硫酸,可以析出硫酸铜晶体,其原因是
▲。
⑷炼钢时,可将铁红投入熔融的生铁中,该过程中主要反应的化学方程式是 ▲。
⑸某硫酸厂为测定反应Ⅳ所得气体中SO2的体积分数,取280mL(已折算成标准状况)气体样品与足量Fe2(SO4)3溶液完全反应后,用浓度为0.02000 mol/L的K2Cr2O7标准溶液滴定至终点,消耗K2Cr2O7溶液25.00 mL 。
已知:Cr2O72-+ Fe2++ H+→Cr 3++
3++  Fe3++ H2O(未配平)
Fe3++ H2O(未配平)
①SO2通入Fe2(SO4)3溶液,发生反应的离子方程式为 ▲。
②反应Ⅳ所得气体中SO2的体积分数为 ▲。
CoCl2·6H2O是一种饲料营养强化剂。以含钴废料(含少量Fe、Al等杂质)制取CoCl2·6H2O的一种新工艺流程如下图: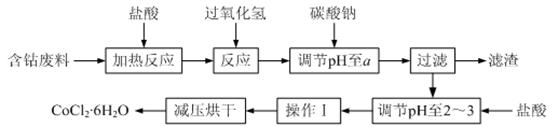
已知:
①钴与盐酸反应的化学方程式为:Co+2HCl=CoCl2+H2↑
②CoCl2·6H2O熔点86℃,易溶于水、乙醚等;常温下稳定无毒,加热至1 10
10 ~120℃时,失去结晶水变成有毒的无水氯化钴。
~120℃时,失去结晶水变成有毒的无水氯化钴。
③部分阳离子以氢氧化物形式沉淀时溶液的pH见下表:
| 沉淀物 |
Fe(OH)3 |
Fe(OH)2 |
Co(OH)2 |
Al(OH)3 |
| 开始沉淀 |
2.3 |
7.5 |
7.6 |
3.4 |
| 完全沉淀 |
4.1 |
9.7 |
9.2 |
5.2 |
请回答下列问题:
⑴在上述新工艺中,用“盐酸”代替原工艺中“盐酸与硝酸的混酸”直接溶解含钴废料,其主要优点为 ▲。
⑵加入碳酸钠调节pH至a,a的范围是 ▲。
⑶操作Ⅰ包含3个基本实验操作,它们是 ▲和过滤。
⑷制得的CoCl2·6H2O需减压烘 干的原因是 ▲。
干的原因是 ▲。
⑸为测定产品中CoCl2·6H2O含量,某同学将一定量的样品溶于水,再向其中加入足量的AgNO3溶液,过滤,并将沉淀烘干后称量其质量。通过计算发现产品中CoCl2·6H2O的质量分数大于100%,其原因可能是 ▲。
⑹在实验室中,为了从上述产品中获得纯净的CoCl2·6H2O,采用的方法是 ▲。
某些废旧塑料可采用下列方法处理:将废塑料隔绝空气加强热,使其变成有用的物质,实验装置如右图。加热聚丙烯废塑料得到的产物如下表:
| 产物 |
氢气 |
甲烷 |
乙烯 |
丙烯 |
苯 |
甲苯 |
碳 |
质量分 数(%) 数(%) |
12 |
24 |
12 |
1 6 6 |
20 |
10 |
6 |
(1)试管A中残余物有多种用途,如下列转化就可制取高聚物聚乙炔。
A中残留物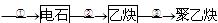
写出反应②和③的化学方程式, 。
(2)试管B收集到的两种产品中,有一种能使酸性高锰酸钾溶液褪色的物质,其一氯代物有_____________种。
(3)锥形瓶C中观察到的现象 。经溴水充分吸收,剩余气体经干燥后的平均相对分子质量为__________________。
。经溴水充分吸收,剩余气体经干燥后的平均相对分子质量为__________________。
(4)写出C中逸出的气体在工业上的两种用途__________________、__________________。
有机玻璃是一种重要的塑料,有机玻璃的单体A(C5H8O2)不溶于水,并可以发生以下变化,请回答: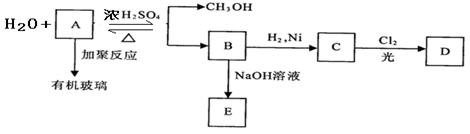
(1) B分子中含有的官能团名称是_____________, _____________。
(2) 由B转化为C的反应属于(选填序号) _____________。
① 氧化反应② 还原反应③ 加成反应 ④ 取代反应
④ 取代反应
(3) C的一氯代物D有两种,C的结构简式是_____________。
(4) 由A生成B的化学方程式是___________________________ ________________。
________________。
(5) 有机玻璃的结构简式是____________________________________。
在一定温度下,将2mol A和2mol B两种气体相混合于体积为
2 L的某密闭容器中(容积不变),发生如下反应:3A(g)+B(g) x C(g)+2D(g)
x C(g)+2D(g)  H <0, 2min末反应达到平衡状态(温度不变),生成了0
H <0, 2min末反应达到平衡状态(温度不变),生成了0 .8 mol D,并测得C的浓度为0.4 mol/L,请填写下列空白:
.8 mol D,并测得C的浓度为0.4 mol/L,请填写下列空白:
(1)X的值等于。
(2)计算该反应的化学平衡常数K=,升高温度时K值
将(选填“增大”、“减小”、“不变”)。
(3)A的物质的转化率为。
(4)若维持温度不变,在原平衡混合物的容器中再充入3mol C和3mol D,欲使达到新的平衡时,各物质的物质的量分数与原平衡相同,则至少应再充入B的物质的量为mol;达新平衡时,A的物质的量为n(A)= mol。