现有①NaCl ②金刚石 ③NH4Cl ④Na2SO4 ⑤干冰 ⑥NaOH六种物质,按下列要求回答:(注意(1)(3)两小题用序号填入)
(1)属于离子化合物的是 ,只有离子键的物质是 ,
晶体以分子间作用力结合的是 。
(2)①的电子式是__ _____,⑤的电子式是__ ______。
(3)熔化时不需要破坏化学键的是 ,熔化时需要破坏共价键的是_______,
硬度最高的是 ,熔点最低的是 。
(7分)现有五种短周期元素的性质、用途或原子结构信息如下表:
| 元素 |
元素的性质、用途或原子结构信息 |
| Q |
原子核外有6个电子 |
| R |
最外层电子数是次外层电子数的3倍 |
| X |
气态氢化物的水溶液常用作肥料,呈弱碱性 |
| Y |
第三周期元素的简单阴离子中离子半径最小 |
| Z |
单质为银白色固体,在空气中燃烧发出黄色火焰 |
请根据表中信息回答下列问题:
(1)Q最简单的气态氢化物分子的空间构型为________。
(2)R单质与X单质在雷电条件下反应产物为________化合物(填“共价”或“离子”)。
(3)写出R与Z组成仅含离子键的化合物的化学式:______________。
(4)工业上用电解Y与Z形成化合物的水溶液制取Y单质,写出该反应的离子方程式:_______________。
(5)在1.01×105Pa、298 K时,1.4 g QR气体在1.6 g R2气体中完全燃烧,生成QR2气体时放出14.15 kJ热量,写出QR的燃烧热化学方程式:____________________________。
某亚硝酸钠生产厂采用硝酸为原料,其生产原理是NO+NO2+2NaOH===2NaNO2+H2O。工艺流程如下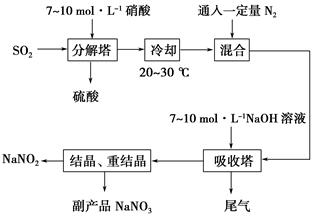
(1)分解塔中填有大量的瓷环,其目的是:_____________________________。
(2)按一定计量比在反应塔中通SO2和喷入硝酸,若反应后生成的NO与NO2物质的量之比恰好1∶1,则分解塔中发生反应的化学方程式为: ____________________________。试从产物产率的角度分析该反应中硝酸的浓度不宜过大或过小的原因是_____________________________________,若硝酸浓度过高,吸收塔中可能发生的副反应化学方程式为_____________________________________________。
(3)通入一定量的N2的目的是: ___________________________________。
(4)吸收塔中尾气如何再利用:_______________________________________。
下列框图涉及到的物质所含元素中,除一种元素外,其余均为1~18号元素。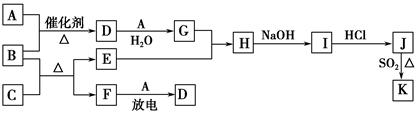
已知:A、F为无色气体单质,B为具有刺激性气味的气体,C为黑色氧化物,E为红色金属单质(部分反应的产物未列出)。请回答下列问题:
(1)F的组成元素在元素周期表中的位置______________。
(2)E与G的稀溶液反应的离子方程式为______________________。
(3)B和C反应的化学方程式为____________________________________。
(4)J、K是同种金属的不同氯化物,K为白色沉淀。写出SO2还原J生成K的离子方程式______________。
正确书写下列化学反应的离子方程式
(1)Cl2和石灰乳的反应:_______________________________________________;
(2)把H2SO4、Na2SO3、Na2S三种溶液混合:________________________________________;
(3)向漂白粉溶液中通入少量SO2气体:______________________________________________;
(4)工业制粗硅的化学方程式:_____________________________________________________;
(5)将盐酸滴入Fe(NO3)2溶液中:___________________________________________________。
(10分) 1.92gCu片与一定量的浓HNO3作用,当收集到NO2和NO气体共1.12L时(标准状况),金属铜恰好全部作用。则:
(1)反应中消耗HNO3______mol,转移电子______mol。
(2)用排水法收集生成的气体,最后气体的体积为L。(标况)
(3)向收集到的气体中通入ml O2(标况)才能使水刚好充满整个集气容器。