钡盐行业生产中排出大量的钡泥[主要含有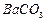 、
、 、
、 、
、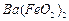 等。某主要生产
等。某主要生产 、
、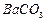 、
、 的化工厂利用钡泥制取
的化工厂利用钡泥制取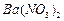 ,其部分工艺流程如下:
,其部分工艺流程如下:
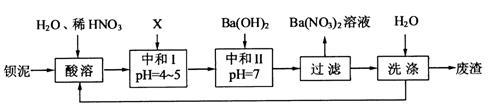
(1)酸溶后溶液中 ,
,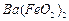 与
与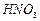 的反应化学方程式为 。
的反应化学方程式为 。
(2)酸溶时通常控制反应温度不超过70℃,且不使用浓硝酸,
原因是 、 。
(3)该厂结合本厂实际,选用的X为 (填化学式);中和Ⅰ使溶液中 (填离子符号)的浓度减少(中和Ⅰ引起的溶液体积变化可忽略)。
(4)上述流程中洗涤的目的是 。
直接排放含SO2的烟气会形成酸雨,危害环境。利用钠碱循环法可脱除烟气中的SO2.。
(1) 在钠碱循环法中,Na2SO3溶液作为吸收液,可由NaOH溶液吸收SO2制得,该反应的离子方程式是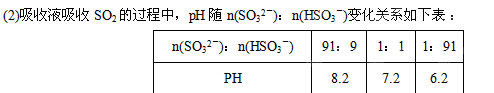
①由上表判断NaHSO3溶液显性,用化学平衡原理解释:
②当吸收液呈中性时,溶液中离子浓度关系正确的是(选填字母):
a.c(Na+) = 2c(SO32-)+c(HSO3-)
b.c(Na+)>c(HSO3-)>c(SO32-)>c(H+) = c(OH-)
c.c(Na+)+c(H+)=c(SO32-)+c(HSO3-)+c(OH-)
盐碱地(含较多NaCl、Na2CO3)不利于作物生长,通过施加适量石膏可以降低土壤的碱性。试用化学方程式分别表示盐碱地产生碱性的原因:,及用石膏降低其碱性的反应原理:。
请判断下列说法是否正确(填“对”或“错”)。
(1)碱性锌锰电池是一次电池,铅蓄电池是二次电池。
(2)随着温度的升高,纯水的pH增大。
(3)冰醋酸、纯碱、小苏打分别属于酸、碱、盐。
(4)镀锌铁制品破损后,镀层仍能保护铁制品。
(5)醋酸在醋酸钠溶液中电离的程度大于在纯水中电离的程度。
(6)25 ℃时,某物质的溶液pH<7,则该物质一定是酸或强酸弱碱盐。
(7)用Na2S去除废水中的Hg2+:Hg2++S2-=HgS↓
(8)pH=2与pH=1的硝酸中c(H+)之比为1:10
(9)Na2CO3溶液中c(Na+)与c(CO32-)之比为2:1
(10)向含有硫酸钙的水垢中加入碳酸钠溶液,沉淀的转化可表示为:
CaSO4(s)  SO42— + Ca2+
SO42— + Ca2+
CO32— CaCO3(s)
CaCO3(s)
常温时,在稀溶液中c(H+)和c(OH-)的乘积总是等于。
(1)酸性溶液c(H+)(填“>”、“<”或“=”,下同)c(OH-),pH 7。
人的胃液中含有盐酸,经测定某人胃液的pH为2,则其中的c(H+)=mol/L。
食醋常用于食品调味,其主要成分为醋酸,醋酸的电离方程式为。
(2)室温下,pH均为3的盐酸和醋酸溶液,下列各项中相等的是(填序号)。
①溶液中c(H+)②酸的物质的量浓度③完全中和时,消耗NaOH的质量
(3)在①NaCl、②CH3COONa、③NH4Cl三种盐溶液中,常温下呈酸性的是(填序号,下同)), 呈中性的是, 呈碱性的是。
(4)氯化铁水解的离子方程式为,配制氯化铁溶液时滴加少量盐酸的作用是。
25℃时,现有浓度均为0.10 mol/L的两种溶液:① (NH4)2SO4溶液、② Na2SO4溶液。请回答:
(1)两种溶液中,pH<7的是(填“①”或“②”),其原因是(用离子方程式表示)。
(2)下列说法正确的是(填序号)。
① (NH4) 2SO4是弱电解质
② (NH4) 2SO4和Na2SO4均能促进水的电离
③两种溶液等体积混合后,溶液中离子浓度大小关系为:c(Na+)= c(SO42-)>c(NH4+)>c(H+)>c(OH-)