[化学-物质结构与性质]
(1)中国古代四大发明之一——黑火药,它的爆炸反应为

①除S外,上列元素的电负性从大到小依次为 。
②在生成物中,A的晶体类型为 ,含极性共价键的分子的中心原子轨道杂化类型为 。
③已知 与
与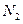 结构相似,推算HCN分子中
结构相似,推算HCN分子中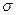 键与
键与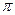 键数目之比为 。
键数目之比为 。
(2)原子序数小于36的元素Q和T,在周期表中既处于同一周期又位于同一族,且原子序数T比Q多2。T的基态原子外围电子(价电子)排布为 ,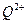 的未成对电子数是 。
的未成对电子数是 。
(3 )在
)在 的水溶液中,一定条件下存在组成为
的水溶液中,一定条件下存在组成为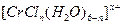 (n和x均为正整数)的配离子,将其通过氢离子交换树脂(R-H),可发生离子交换反应:
(n和x均为正整数)的配离子,将其通过氢离子交换树脂(R-H),可发生离子交换反应:
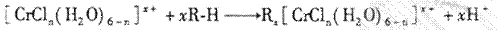
交换出来的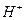 经中和滴定,即可求出x和n,确定配离子的组成。
经中和滴定,即可求出x和n,确定配离子的组成。
将含0.0015 mol 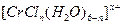 的溶液,与R-H完全交换后,中和生成的
的溶液,与R-H完全交换后,中和生成的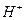 需浓度为0.1200 mol·L-1 NaOH溶液25.00 ml,该配离子的化学式为 。
需浓度为0.1200 mol·L-1 NaOH溶液25.00 ml,该配离子的化学式为 。
(6分)下图表示Zn投入一定浓度一定体积的稀H2SO4溶液中后,反应时间与生成H2的体积的图象。(纵坐标为H2的生成速率)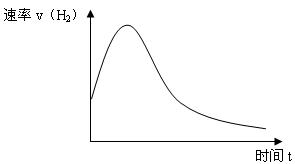
(1)反应前期速率加快的原因是:。
(2)反应后期速率下降的原因是:。
(3)为了减缓上述反应的速率,欲向溶液中加入下列物质,你认为可行的是:。
| A.蒸馏水 | B.氯化钠固体 | C.氯化钠溶液 | D.浓盐酸 |
(1)冶炼金属常用以下几种方法:①还原法,②电解法,③热分解法。下列金属各采用哪种方法还原最佳。(用序号填写下列空白。)
Ⅰ.Fe、Zn、Cu 等中等活泼金属。
等中等活泼金属。
Ⅱ.Na 、Mg、Al等活泼或较活泼金属。
、Mg、Al等活泼或较活泼金属。
Ⅲ.Hg、Ag等不活泼金属。
(2)写出以锌片、铜片为两极,稀硫酸溶液为电解质溶液组成的原电池的电极反应式:
负极:;正极:。
A、B、C、D、E、F六种短周期元素的原子序数依次增大,已知:①A原子核内只有1个质子;②B原子最外层电子数是次外层电子数的2倍;③C原子最外层电子数比次外层电子数多4个;④D原子的次外层电子数是最外层电子数的8倍;⑤E单质既能和盐酸反应,又能和烧碱反应;⑥F与C同主族。用化学符号回答下列问题:
(1)用电子式表示下列物质A2C2,DCA_________________;
(2)写出E与烧碱反应的离子方程式。
(3)写出DCA与B的最高价氧化物反应的化学方程式:
。
已知:甲、乙、丙为常见单质,甲常温下为固体,乙为一黄绿色气体,丙为无色气体。A、B、C、D均为化合物,D为一红褐色沉淀,它们之间有下图转化关系。请回答以下问题。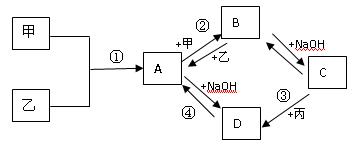
(1)写出下列物质的化学式;乙;B。
(2)写出③反应的化学方程式:。
(3)写出②反应的离子方程式:。
下列关于实验现象的描述,正确的是
①由铜锌组成的原电池,电子是从锌经过导线流向铜
②把铜片和锌片紧靠在一起浸入稀硫酸中,铜表面出现气泡
③把铜片插入三氯化铁溶液中,在铜片表面出现一层铁
④把锌片放入盛盐酸的试管中,加入几滴氯化铜溶液,产生气泡的速率加快