目前世界上60%的镁是从海水提取的。海水提镁的主要流程如下: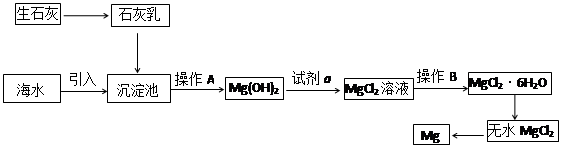
请回答下列问题:
⑴从离子反应的角度思考,在海水中加入石灰乳的作用是 。
⑵石灰乳是生石灰与水形成的混合物,从充分利用海洋化学资源,提高经济效益的角度,生产生石灰的主要原料来源于海洋中的 。
⑶操作A是 , 操作B是 。
⑷无水MgCl2在熔融状态下,通电后会生成Mg和Cl2,该反应的化学方程式是 。从考虑成本和废物循环利用的角度,副产物氯气可以用于 。
⑸海水提镁的过程,为什么要将海水中的氯化镁转变为氢氧化镁,再转变为氯化镁?
。
( 8 分)如图A为直流电源,B为浸透饱和氯化钠溶液和酚酞试液的滤纸,c、d为两个铂片,C为电镀槽,接通电路后,发现B上的c点显红色,请填空: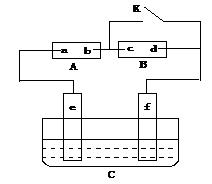
(1)电源A上的a为_____极
(2)滤纸B上发生的总化学方程式为:_______________________________
(3)欲在电镀槽中实现铁上镀铜,接通K点,使c、d两点短路,则电极e上发生的反应为:____________ ____ ,C中盛放的电镀液可以是______溶液。
( 8 分)采用惰性电极从NO3-、SO42-、Cl-、Cu2+、Na+、Ag+、H+ 选出适当离子组成的电解质(非熔融态下),并电解其水溶液
(1)若两极分别放出H2和O2,电解质可能为。
(2)若阴极析出金属,阳极放出O2,电解质可能为。
(3)若两极分别放出气体,且体积比为 ,电解质可能为。
,电解质可能为。
(4)若既无O2也无 H2放出,则电解质可能为。
H2放出,则电解质可能为。
(10分)按要求对下图中两极进行必要的连接并填空:
(1)在A图中请加以必要连接,使锌片不断损耗,铜片上冒H2气泡。则连接后的装置叫。
电极反应式:锌板:;铜板:。
(2)在B图中a、b均是惰性电极,加以必要的连接后,使a极析出铜, b极放出气体。该装置叫。
电极反应式:a极:b极:。
经过一段时间后,停止反应并搅均溶液,溶液的pH值(填 “升高、降低或不变”),加入一定量的后,溶液能恢复至与电解前完全一致。
( 6 分)回答下列问题:
(1)反应A(g)+B(g) C(g)+D(g)过程中的能量变化如右图所示,判断该反应△H0(填“>”、“<”、“无法确定”)。
C(g)+D(g)过程中的能量变化如右图所示,判断该反应△H0(填“>”、“<”、“无法确定”)。
(2)在Al2O3、Ni催化下气态甲酸发生下列反应:
甲酸(g)=" CO" (g)+ H2O (g) △H1=" +" 34.0 kJ/mol
甲酸(g)= CO2 (g)+ H2(g)△H2= —7.0 kJ/mol
则甲酸的分子式为,在该条件下,气态CO2和气态H2生成气态CO和气态H2 O的热化学方程式为。
O的热化学方程式为。
(3)火箭推进器中盛有强还原剂液态肼(N2H4)和强氧 化剂液态双氧水(H2O2)。
化剂液态双氧水(H2O2)。
当把0.4mol液态肼和0.8mol 液态H2O2混合反应,生成氮气和水蒸气,放出256.7kJ
的热量(相当于25℃、101 kPa下测得的热量)。反应的热化学方程式为
。
(本小题共15分)乙基香兰素是当今世界上最重要的合成香料之一,其结构简式如下图所示。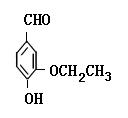
(1)以下推测正确的是( 填字母)。
填字母)。
| A.从分子结构上看,它应该属于芳香烃 |
| B.该物质的一个分子内含有一个碳氧双键、三个碳碳双键 |
| C.1 mol该物质最多能与4molH2发生加成反应 |
| D.该物质能与碳酸钠溶液反应产生CO2气体 |
(2)R物质属于乙基香兰素的同分异构体,其分子中苯环上有2个取代基,R可以发生水解反应生成M和N两种有机物。M可与饱和溴水反应生成白色沉淀。N的质谱图相对分子质量为32,且红外光谱图上发现有O-H键、C-H键和C-O键的振动吸收。
试写出符合条件的R的结构简式(任写两种) ;。
(3)X也是乙基香兰素的同分异构体,可以利用X通过不同的反应制得下列物质。
请回答下列问题:
①X中所含官能团的名称是 反应Ⅰ的反应类型是;
②反应Ⅲ所需的试剂是 ;
;
③反应Ⅳ的化学方程式为