根据下图,可判断出下列离子方程式中错误的是()
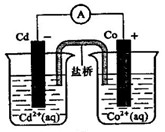

| A. | 2 (s)+ (aq)=2 (aq)+ (s) |
| B. | (aq)+ (s)= (s)+ (aq) |
| C. | 2 (aq)+ (s)=2 (s)+ (aq) |
| D. | 2 (aq)+ (s)=2 (s)+ (aq) |
I2在KI溶液中存在下列平衡:I2(aq)+I-(aq)=I3-(aq) , 某 I2、KI混合溶液中,I3-的物质的量浓度c(I3-)与温度T的关系如图所示(曲线上任何一点都表示平衡状态)。下列说法正确的是: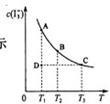
| A.反应I2(aq)+I-(aq)=I3-(aq)的△H>0 |
| B.若温度为T1、T2,反应的平衡常数分别为K1、K2,则K1<K2 |
| C.若反应进行到状态D时,一定有v正>v逆 |
| D.状态A与状态B相比,状态A的c(I2)大 |
下列溶液中微粒的物质的量浓度关系正确的是:
| A.室温下,向0.01mol·L-1NH4HSO4溶液中滴加NaOH 溶液至中性: c(Na+)>c((SO42-)>c(NH4+)>c(OH-)=c(H+) |
| B.0.1mol·L-1NaHCO3溶液: c(Na+)>c(OH-)>c((HCO3-)>c(H+) |
| C.Na2CO3溶液:c(OH-)-c(H+)=c(HCO3-)+ 2c(H2CO3) |
| D.25℃时,,pH=4.75、浓度均为0.1mol·L-1的CH3COOH 、CH3COONa 混合溶液:c(CH3COO-)+c(OH-)<c(CH3COOH)+c(H+) |
下列有关离子检验的操作和实验结论都正确的是(
| 选项 |
实验操作及现象 |
实验结论 |
| A |
向某溶液中加入氯化钡溶液,有白色沉淀生成,再加盐酸酸化,沉淀不溶解 |
该溶液中一定含有SO42- |
| B |
向某溶液中加入足量的盐酸无明显现象,再加入BaCl2溶液,产生白色沉淀 |
原溶液中一定含有SO42- |
| C |
向某溶液中加入稀盐酸,产生能使澄清石灰水变浑浊的无色无味气体 |
该溶液中一定含有CO32- |
| D |
用铂丝蘸取某溶液在无色火焰上灼烧直接观察火焰颜色未见紫色 |
原溶液中不含K+ |
阿司匹林是日常生活中应用广泛的医药之一。它可由下列方法合成:
下列说法正确的是
| A.邻羟基苯甲醛分子中所有的原子可能在同一平面 |
| B.用酸性KMnO4溶液直接氧化邻羟基苯甲醛可实现反应① |
| C.反应②中加入适量的NaHCO3可提高阿司匹林的产率 |
| D.与邻羟基苯甲酸互为同分异构体,苯环上一氯代物仅有2种且能发生银镜反应的酚类化合物共有3种 |
下列关于反应过程中能量变化的说法正确的是
A.右图中a、b曲线可分别表示反应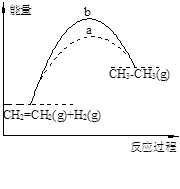 CH2=CH2(g)+H2(g)→CH3CH3(g) ΔH<0 使用和未使用催化剂时,反应过程中的能量变化 |
| B.己知2C(s)+2O2(g)=2CO2(g)ΔH1; 2C(s)+O2(g)=2CO(g)ΔH2则ΔH1>ΔH2 |
| C.同温同压下,反应H2(g)+Cl2(g)=2HCl(g)在光照和点燃条件下的ΔH相同 |
| D.在一定条件下,某可逆反应的ΔH=+100kJ·mol-1,则该反应正反应活化能比逆反应活化能大100kJ·mol-1 |