用离子方程式表示下列反应:
(1)某可溶性盐的化学式XmYn(是最简结构m≠n),将一定量的该盐溶于足量的水中,若测得溶液的pH为3,该盐水解的离子方程式可能为 。若测得溶液的pH为11,则该盐与水反应的离子方程式可能为 。
(2)NH4Cl溶液与Na反应 。
(3)AlCl3溶液与Na2S反应 。
(4)CuSO4溶液与Na2S溶液反应 。
利用太阳能分解水产生H2,在催化剂作用下H2与CO2反应合成CH3OH,并开发出直接以甲醇为燃料的燃料电池。已知:H2(g)+1/2O2(g)=H2O(l) ΔH=-285.8 kJ·mol-1、CH3OH(l)+ 3/2O2(g)= CO2 (g)+ 2H2O(l)ΔH=-726.5 kJ·mol-1、CO(g) +1/2O2(g)= CO2 (g)ΔH=-283.0 kJ·mol-1。
请回答下列问题:
⑴用太阳能分解18g水,需要消耗的能量为kJ。
⑵ 液态CH3OH不完全燃烧生成CO和液态H2O的热化学方程式为。
⑶CO2合成燃料CH3OH是碳减排的新方向。在容积为2 L的密闭容器中,充2 mol CO2和6 mol H2,由CO2和H2合成甲醇,反应式:CO2(g)+3H2(g) CH3OH(g)+H2O(g),在其他条件不变的情况下,考察温度对反应的影响,实验结果如下图所示(注:T1、T2均大于300 ℃):
CH3OH(g)+H2O(g),在其他条件不变的情况下,考察温度对反应的影响,实验结果如下图所示(注:T1、T2均大于300 ℃):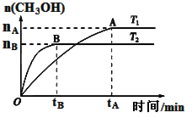
①下列说法正确的是
A.温度为T2时,从反应开始到平衡,生成甲醇的平均速率为: v(CH3OH)=nB/tBmol·(L·min)-1
B.T2>T1,T2平衡时,甲醇产量变少,所以该反应为放热反应
C.该反应在T2时的平衡常数比T1时的平衡常数大
D.处于A点的反应体系从T1变到T2,平衡逆向移动
②能判断该反应已达化学反应限度标志的是(填字母。
A.H2的百分含量保持不变
B.容器中CO2 浓度与H2浓度之比为1: 3
C.容器中混合气体的密度保持不变
D.CO2消耗速率与CH3OH生成速率相等
⑷科学家致力于CO2的“组合转化”技术研究,如将CO2和H2以体积比1∶4比例混合通入反应器,适当条件下,反应可获得一种能源。完成以下化学方程式,就能知道该种能源。
CO2+4H2 2H2O + 。
2H2O + 。
⑸ 在直接以甲醇为燃料的燃料电池中,电解质溶液为酸性,总反应式为:2CH3OH + 3O2=2CO2+4H2O,则正极的反应式为;负极的反应式为。
已知可逆反应CO2(g) + H2(g) CO(g) + H2O(g),
CO(g) + H2O(g),
⑴写出该反应的化学平衡常数表达式:K=。
⑵830K时,若起始时:c (CO2)=2mol/L,c (H2)=3mol/L,平衡时CO2的转化率为60%,氢气的转化率为;K值为。
⑶830K时,若只将起始时c (H2)改为6mol/L,则氢气的转化率为。
⑷若830K时,起始浓度c (CO2) =" a" mol/L,c (H2) =" b" mol/L,H2O的平衡浓度为c (H2O) =" c" mol/L,则:①a、b、c之间的关系式是 ;②当a = b时,a =c。
红磷P(s)和Cl2(g)发生反应生成PCl3(g)和PCl5(g)。反应过程和能量关系如图所示( 图中的△H表示生成1mol产物的数据)。根据图示,回答下列问题:
⑴P和Cl2反应生成PCl3(g)的热化学方程式。
⑵PCl5(g)分解成PCl3(g)和Cl2的热化学方程式。
⑶白磷能自燃,红磷不能自燃。白磷转变成红磷为(“放”或“吸”) 热反应。如果用白磷替代红磷和Cl2反应生成1molPCl5的△H3,则△H3△H1 (填“<”、“>” 或 “=”)。
可逆反应aA(g) + bB(g) cC(g) + dD(g) ,反应时间与C%(产物C的体积分数)函数关系如图所示。A图表示的是温度不同的曲线,B图表示压强不同的曲线,C图表示使用催化剂和不使用催化剂时的反应曲线。
cC(g) + dD(g) ,反应时间与C%(产物C的体积分数)函数关系如图所示。A图表示的是温度不同的曲线,B图表示压强不同的曲线,C图表示使用催化剂和不使用催化剂时的反应曲线。
试比较下列大小关系:T1T2, P1P2, ΔH0,ΔS0。使用催化剂的是反应线。
按要求完成下列问题:
⑴某有机物的键线式是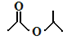 ,请写出它与NaOH溶液反应的化学方程式:
,请写出它与NaOH溶液反应的化学方程式:
⑵DDT人类合成的第一种有机氯农药,其分子结构球棍模型如图所示。请分析该物质的核磁共振1H谱图中有个吸收峰。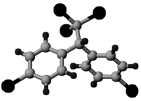
⑶F和G(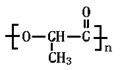 ) 是日常生活中常用的两种合成高分子材料,可由某烃经下列反应得到。
) 是日常生活中常用的两种合成高分子材料,可由某烃经下列反应得到。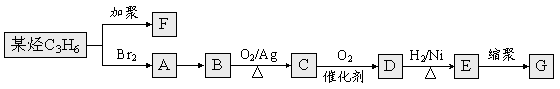
请回答下列问题:
①F的结构简式为。
②C中所含官能团的名称为,用仪,可以测定D中所含官能团。
③A→B的化学方程式为。
④已知2RCH(OH)COOH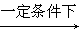 2H2O +
2H2O + 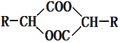
请参考题目中的合成途径,若合成 ,起始原料的某烃的结构简式为,最少用步反应,可以合成产物。
,起始原料的某烃的结构简式为,最少用步反应,可以合成产物。