NaH2PO4是一种用途广泛的化工产品。工业上主要是以烧碱(或纯碱)中的磷酸生产,若能用氯化钠取代烧碱或纯碱来制取,则可使生产成本大大降低。但在通常条件下,氯化钠与磷酸之间的复分解反应不能自发进行,有研究者设计了用萃取法制取NaH2PO4的工艺:
萃取时主要反应如下:(S代表萃取剂,萃取剂对HCl的选择性比H3PO4好,主要萃取HCl)
①NaCl+H3PO4  NaH2PO4+HCl
NaH2PO4+HCl
②HCl+S  HCl·S △H<0
HCl·S △H<0
③H3PO4+S  H3PO4·S △H<0
H3PO4·S △H<0
(1)向H3PO4和NaCl溶液中加入萃取剂S后需要不断搅拌,搅拌的作用是 。
(2)向操作I后所得的油层中加入适量氨水的目的是 。
(3)下图是萃取温度对HCl萃取率的影响和H3PO4与NaCl物质的量比对HCl萃取率的影像图。
①当萃取温度低于40时,温度越低,萃取剂黏度越大,不利于HCl的萃取;当温度高于40℃时,HCl萃取率降低的原因是 。
②从H3PO4与NaCl物质的量比对HCl萃取率的影像图中可以看出,适当提高H3PO4与NaCl物质的量比,会促进HCl的萃取。但H3PO4过量太多,会导致HCl的萃取率降低,其原因是 。
(4)萃取法制取NaH2PO4的原理是 。
短周期元素D、E、X、Y、Z原子序数逐渐增大。它们的最简氢化物分子的空间构型依次是正四面体、三角锥形、正四面体、角形(V形)、直线形。回答下列问题:
(1)Z的价电子排布式为________________,EZ3分子的空间构型为_____________________;
(2)X与Z构成的分子是_________分子(填“极性”或“非极性”)。
(3)D和Y形成的化合物,其分子中的共价键为__________共价键(填“极性”或“非极性”),该分子中D原子的杂化方式为____________。
(4)写出一个验证Y与Z的非金属性强弱的离子反应方程式_________________________;
(5)金属镁和E的单质在高温下反应得到的产物与水反应生成两种碱性物质,该反应的化学方程式是_________。
(9分)
(1)CO2的电子式为_________________;属于______________化合物(填“共价”或“离子”;
(2)H2O2的结构式为___________________,属于分子(填“极性”或“非极性”);
(3)SO42-中S原子的杂化方式为,该微粒的空间构型为;
(4)冰的密度比水的密度小的原因是;
(5)NH3极易溶于水的原因是:①_________________________、②______________________;
钢铁很容易生锈而被腐蚀,每年因腐蚀而损失的钢材占世界钢材年产量的四分之一。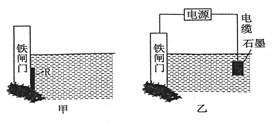
(1)钢铁腐蚀主要是吸氧腐蚀,该腐蚀过程中的电极反应式为________________
(2)为了降低某铁闸门被腐蚀的速率,可以采用上述图甲所示的方案,其中焊接在铁闸门上的固定材料R可以采用____(填序号)。
| A.铜 | B.钠 | C.锌 | D.石墨 |
(3)上图乙所示的方案也可以降抵铁闸门的腐蚀速率,其中铁闸门应该连接在直流电源的_______极。
在某温度下,取一定质量的CuSO4溶液,用石墨做电极进行电解,当阳极产生标准状况下气体1.12 L时,CuSO4恰好被完全电解,得到密度为1.2 g/cm3的溶液200 mL。求:
(1)电解后,所得溶液的pH= 。
(2)电解前,所取CuSO4溶液的质量为 。
(3)若要使电解后所得溶液恢复至电解前的原始状态,需要加入 质量为 。
ZnMnO2干电池应用广泛,其电解质溶液是ZnCl2NH4Cl混合溶液。
(1)该电池的负极材料是________。电池工作时,电子流向________(填“正极”或“负极”)。
(2)若ZnCl2NH4Cl混合溶液中含有杂质Cu2+,会加速某电极的腐蚀,其主要原因是____________。
欲除去Cu2+,最好选用下列试剂中的________(填代号)。
| A.NaOH | B.Zn | C.Fe | D.NH3·H2O |
(3)MnO2的生产方法之一是以石墨为电极,电解酸化的MnSO4溶液。阴极的电极反应式是___________。若电解电路中通过2 mol电子,MnO2的理论产量为________g。