下图纵坐标表示沉淀的质量,横坐标表示所加试剂的体积,请选出有对应的曲线变化关系的实验项( )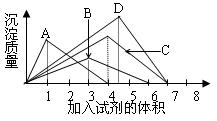
| A.硝酸银溶液中加入氨水溶液 |
| B.往澄清石灰水中逐渐通入CO2气体 |
| C.往AlCl3溶液中逐NaOH溶液 |
| D.往NaAlO2溶液中逐滴加入盐酸溶液 |
下列电离方程式中,正确的是
| A.Ba(OH)2 =Ba2++ (OH)- | B.FeCl3=Fe2++3Cl- |
| C.H2SO4 =H2++SO42- | D.Al2(SO4)3=2Al3++3SO42- |
标准状况下,等体积的NH3和CH4两种气体,下列有关说法错误的是
| A.所含分子数目相同 |
| B.所含氢原子物质的量之比为3:4 |
| C.质量之比为16:17 |
| D.密度之比为17:16 |
等质量的钠进行下列实验,最终生成氢气最多的是()
| A.将钠投入到足量水中 | B.将钠用铝箔包好并刺一些小孔,再投入足量水中 |
| C.将钠投入足量稀硫酸中 | D.将钠投入足量饱和食盐水中 |
以下是对某水溶液进行离子检验的方法和结论,其中正确的是()
| A.滴加适量氯水不发生颜色变化,再加入KSCN溶液,溶液立即呈红色。原溶液中一定含有Fe2+ |
| B.加入足量的CaCl2溶液,产生了白色沉淀。溶液中一定有大量的CO32- |
| C.用洁净的铂丝蘸取该溶液,置于火焰上灼烧,透过蓝色钴玻璃能观察到火焰呈紫色。该溶液中一定含有钾离子,可能含有钠离子。 |
| D.先加适量的盐酸将溶液酸化,再加AgNO3溶液,产生了白色沉淀。溶液中一定含有大量的Cl- |
下列离子方程式书写正确的是()
| A.金属钠溶于水:2Na+2H2O =2Na++2OH—+H2↑ |
| B.氯化铝溶液与足量氨水反应:Al3+ + 4OH- =AlO2- +2H2O |
| C.硫酸铜溶液与氢氧化钡溶液反应:Cu2+ +2OH- =Cu(OH)2↓ |
| D.铁与稀硫酸反应:2Fe +6H+ =2Fe3++3H2↑ |