是一种可降解的聚碳酸酯类高分子材料,由于其具有优良的耐冲击性和韧性,因而得到了广泛的应用。以下是某研究小组开发的生产的合成路线:

已知以下信息:
①可使溴的溶液褪色;
②中有五种不同化学环境的氢;
③可与溶液发生显色反应;
④不能使溴的褪色,其核磁共振氢谱为单峰。
请回答下列问题:
(1)的化学名称是;
(2)的结构简式为;
(3)与反应生成的化学方程式为;
(4)有多种同分异构体,其中能发生银镜反应的是 (写出结构简式);
(5)的同分异构体中含有苯环的还有种,其中在核磁共振氢谱中出现丙两组峰,且峰面积之比为3:1的是(写出结构简式)。
(12分)如图甲、乙是电化学实验装置.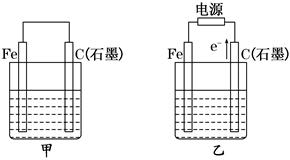
(1)若甲、乙两烧杯中均盛有NaCl溶液。
①甲中石墨棒上的电极反应式为_______________________________________;
②乙中总反应的离子方程式为_____________________________________ ____;
____;
③将湿润的淀粉KI试纸放在乙烧杯上方,发现试纸先变蓝后褪色,这是因为过量的Cl2氧化了生成的I2。若反应中Cl2和I2的物质的量之比为5∶1,且生成两种酸,该反应的化学方程式为________________________。
(2)若甲、乙两烧杯中均盛有CuSO4溶液.
①甲中铁棒上的电极反应式为___________________________________。
②如果起始时乙中盛有200 mL pH=5的CuSO4溶液(25℃),一段时间后溶液的pH变为1,若要使溶液恢复到电解前的状态,可向溶液中加入________(填写物质的化学式)________ g。
甲、乙、丙、丁四种短周期元素可以组成下列框图中除Br2和L以外的物质,其原子序数依次增大。甲和乙可形成常见液态化合物K,固体A中含有丙元素的正一价阳离子,其电子层结构与氖原子相同,丁元素原子的最外层电子数是其电子层数的2倍。在一定条件下,下列各物质可发生如图所示的变化(反应中生成的水没有写出):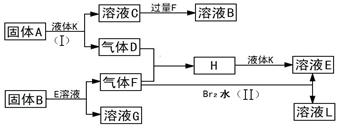
试回答:
(1)甲元素的名称为,溴元素在周期表的位置丁元素的阴离子结构示意图为。
(2)A的电子式为;所含化学键类型为。
(3)乙、丙、丁三元素的离子半径由大到小的顺序为(用元素符号表示)。
(4)反应(I)的化学方程式为。
(5)反应(II)的离子方程式为。
海水占地球总储水量的97.2%。若把海水淡化和化工生产结合起来,既可以解决淡水资源缺乏的问题,又可以充分利用海洋资源。
⑴海水中含有大量的氯化钠。请写出氯离子结构示意图。
⑵目前国际上实用的“海水淡化”主要技术之一是蒸馏法。蒸馏法是将海水变成蒸汽,蒸汽经过冷却而得高纯度淡水,由此可判断蒸馏法是(填物理变化、化学变化)。
⑶工业上利用电解饱和食盐水可制得重要化工产品,又称为“氯碱工业”。电解饱和食盐水的化学方程式为;电解时与电源正极相连的电极上产生的气体是,常用检验该气体。
⑷洪灾过后,饮用水的消毒杀菌成为抑制大规模传染性疾病爆发的有效方法之一。漂白粉是常用的消毒剂。
①工业上将氯气通入石灰乳[Ca(OH)2]制取漂白粉,写出化学反应方程式并用双线桥标出电子转移情况。
②漂白粉的有效成分是(填化学式)。
⑸某NaCl溶液物质的量浓度为a mol·L-1,对应溶液中溶质的质量分数为ω1;若物质的量浓度为b mol·L-1,则对应溶液中溶质的质量分数为ω2;假如b="=" 2 a,则ω22ω1(填:大于、小于、等于)
有一包白色固体,可能含有CaCO3、Na2SO4、KNO3、CuSO4、BaCl2五种物质中的一种或几种。现进行如下实验:
⑴取少量固体粉末加到足量水中,得到白色沉淀,上层为无色清液。
⑵继续往其中加入足量稀硝酸,白色沉淀完全消失,并有气泡产生。
⑶取少量(2)中的溶液滴加Ba(NO3)2溶液,有白色沉淀生成,再加入稀硝酸,沉淀不溶。
根据上述实验现象判断:该白色固体中一定含有,一定不含有,可能含有。
⑷检验可能含有的物质是否存在的实验方法。
同温同压下,同体积的氨气和硫化氢气体的质量比是,密度比是;同质量的氨气和硫化氢气体的体积比是,两者所含氢原子个数比是。