五种元素A、B、C、D、E位于元素周期表的前四周期,已知它们的核电荷数依次增加,A是宇宙中含量最多的元素;B原子的L层p轨道中有2个电子;C与B原子的价层电子数相同;D原子M层的d轨道有一个成对电子;E原子的L层电子数与最外层电子数之比为4:1,其d轨道中的电子数与最外层电子数之比为5:1。
(1)B与A形成只含一个中心原子的共价化合物,其分子的电子式为 ,中心原子的杂化轨道类型是 ,其分子的的立体构型是
(2)A的氧化物与B的氧化物中,分子极性较小的是(填分子式)__________
(3)B与C比较,电负性较大的(填元素名称)____________
(4)写出D的价层电子排布式
(5)E与Al的化学性质相似,请写出E与NaOH溶液反应的化学方程式
(6)写出D的最高价氧化物与盐酸反应的离子方程式
已知如图所示的可逆反应: A(g)+B(g) 2C(g) +D(g);ΔH =" Q" kJ/mol
2C(g) +D(g);ΔH =" Q" kJ/mol
请回答下列问题:
(1)Q0(填“>”、“<”或“=”)
(2)在某温度下,反应物的起始浓度分别为:c(A)=" 1.0" mol/L, c(B)="2.0" mol/L ;达到平衡后,A的转化率为50%,此时B的转化率为;
(3)若反应温度升高,A的转化率(填“增大”“减小”或“不变”);
(4)若反应温度不变,反应物的起始浓度分别为:c(A)=" 3" .0mol/L,
c(B)=" a" mol/L;达到平衡后,c(D)="1.0" mol/L,a=;
(5)反应体系中加入催化剂,反应速率增大,则E1的变化是:E1_______,ΔH的变化是:ΔH________(填“增大”“减小”“不变”)。
由于温室效应和资源短缺等问题,如何降低大气中的CO2含量并加以开发利用,引起了各国的普遍重视。目前工业上有一种方法是用CO2生产燃料甲醇。
(1)在250C、101KPa时,3.2克甲醇(CH30H)完全燃烧生成CO2和液态水时放热72.576kJ,则能表示甲醇燃烧的热化学方程式为___________________。
(2)为探究反应原理,现进行如下实验,在体积为2 L的密闭容器中,充入2mol CO2和6mol H2,一定条件下发生反应:CO2(g)+3H2(g) CH3OH(g)+H2O(g) △H=—49kJ/mol,测得CO2和H2O (g)的浓度随时间变化如图所示。
CH3OH(g)+H2O(g) △H=—49kJ/mol,测得CO2和H2O (g)的浓度随时间变化如图所示。
①从反应开始到平衡,氢气的平均反应速率v(H2)=__________mol/(L·min)。
②下列措施中能使n(H2O)/n(CO2)增大的是________。
A.升高温度 B.再充入3mol H2
C.将CH3OH (g)从体系中分离 D.充入He(g),使体系压强增大
M是生产某新型塑料的基础原料之一,分子式为C10H10O2,分子模型如图所示
(图中球与球之间连线代表化学键单键或双键)。
拟从芳香烃 出发来合成M,路线如下:
出发来合成M,路线如下:
已知:M在酸性条件下水解生成有机物F和甲醇。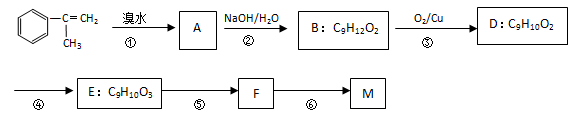
(1)根据分子结构模型写出M的结构简式。
(2)写出②、⑤反应类型分别为、。
(3) D中含氧官能团的名称为,E的结构简式。
(4)写出反应⑥的化学方程式(注明必要的条件)
。
某有机物A的分子式为C3H6O2, A有下列转化关系:(其中F能发生银镜反应)。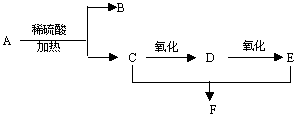
回答下列问题:
(1)A的名称是;
(2)F的结构简式是;
(3)0.1mol D与足量银氨溶液反应,可生成克Ag;
(4)写出A→B + C的化学方程式。
某天然油脂A的化学式为C57H106O6,1mol该油脂在酸性条件下水解可得到1mol甘油、1mol不饱和脂肪酸B和2mol直链饱和脂肪酸C。经测定B的相对分子质量为280,原子个数比为C︰H︰O=9︰16︰1。
(1)写出B的分子式:_________________;C的名称是__________________。
(2)油脂D在酸性条件下水解生成1mol甘油和3mol C,写出油脂D在NaOH溶液中水解的化学方程式。