据悉,奥运会上使用的发令枪所用的“火药”成分是氯酸钾和红磷,经撞击发出响声,同时产生白色烟雾。撞击时发生的化学反应方程式为:5KClO3+6P=3P2O5+5KCl,则下列有关叙述错误的是
| A.上述反应中氧化剂和还原剂的物质的量之比为5∶6 |
| B.上述反应中消耗3 mol P时,转移电子的物质的量为l5 mol |
| C.因红磷和白磷互为同分异构体,所以上述火药中的红磷可以用白磷代替 |
| D.产生白色烟雾是因生成的P2O5白色固体小颗粒吸收空气中的水分生成磷酸小液滴 |
铜锌原电池装置(见图),下列分析正确的是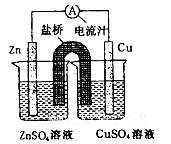
| A.一段时间后两烧杯中c(Zn2+)、c(Cu2+)均减小 |
| B.原电池工作时,Cu电极流出电子,发生氧化反应 |
| C.原电池工作时的总反应为Zn+Cu2+=Zn2++Cu |
| D.盐桥中装有含氯化钾的琼脂,其作用是传递电子 |
室温下,用0.100mol/L 盐酸溶液滴定20.00mL 0.100mol/L的某氨水溶液,滴定曲线如图所示,下列有关说法不正确的是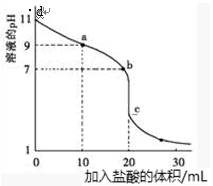
| A.曲线上除d点外任意一点所示溶液中:c(NH4+ )+c(H+)= c(Cl—)+ c(OH-) |
| B.a点所示溶液中, c(Cl— ) > c(NH4+ )> c(NH3·H2O)> c(OH-)> c(H+) |
| C.b点所示溶液中,c(NH4+ )= c(Cl— ) |
| D.c点所示溶液中, c(Cl— ) > c(NH4+ ) > c(H+)>c(NH3·H2O) |
下列关于酸性氧化物、碱性氧化物、单质、混合物的分类中,正确的是
| 酸性氧化物 |
碱性氧化物 |
单质 |
混合物 |
|
| A |
干冰 |
Na2O |
金刚石 |
浓盐酸 |
| B |
CO |
Fe3O4 |
溴 |
漂白粉 |
| C |
SO2 |
Na2O2 |
石墨 |
福尔马林 |
| D |
SO3 |
Fe2O3 |
硫黄 |
FeSO4·7H2O |
【改编】关于Fe(OH)3胶体和MgCl2溶液说法正确的是
| A.都比较稳定,且无色透明 |
| B.可以用是否有丁达尔现象进行鉴别 |
| C.加入NaOH溶液都可产生白色沉淀 |
| D.胶体微粒不可透过滤纸,MgCl2溶液可以 |
某有机物的结构简式为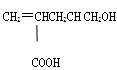 ,下列叙述不正确的是
,下列叙述不正确的是
| A.1mol该有机物能与足量金属钠反应放出1molH2 |
| B.能与乙醇发生酯化反应 |
| C.1mol该有机物在催化剂作用下最多能与1molH2发生还原反应 |
| D.1mol该有机物能与足量NaHCO3溶液反应放出2 molCO2 |