硫酸铜受热分解生成氧化铜和气体,受热温度不同,该气体成分也不同。气体成分可能含SO2、SO3和O2中的一种、二种或三种。某化学课外活动小组通过设计一探究性实验,探索测定反应产生的SO2、SO3和O2的物质的量,并经计算确定各物质的化学计量数,从而确定CuSO4分解的化学方程式。实验可能用到的仪器如下图所示:
【提出猜想】
Ⅰ.所得气体的成分可能只含 一种;
Ⅱ.所得气体的成分可能含有 二种;
Ⅲ.所得气体的成分可能含有 三种。
【实验探究】
实验操作过程(略)。已知实验结束时,硫酸铜完全分解。请回答下列问题:
(1) 请你组装探究实验的装置,按从左至右的方向,各仪器接口连接顺序为:
__ (填序号)
(2) 若实验结束,B中量筒没有收集到水,则证明猜想 正确。
(3)若实验结束,经测定装置C的总质量增加了,能否肯定气体产物中含有SO2而不含SO3?
请说明理由。答:
(4)有两个实验小组进行该实验,由于加热时的温度不同,实验结束后,测得相关数据也不同,数据如下:
| 实验小组 |
称取CuSO4 的质量(g) |
装置C增加 的质量(g) |
量筒中水的体积折算成标 准状况下气体的体积(mL) |
| 一 |
6.4 |
2.56 |
298.7 |
| 二 |
6.4 |
2.56 |
448 |
请通过计算,推断出第一小组和第二小组的实验条件下CuSO4分解的化学反应方程式:
一组:_____________ ;
二组:_ 。
(5)该实验设计中,由于实验操作的原因容易给测定带来最大误差的两个仪器是________和_______(填代号)。
(14分)
Ⅰ:“酒是陈的香”,就是因为酒在储存过程中生成了有香味的乙酸乙酯,在实验室我们也可以用如右图所示的装置制取乙酸乙酯。回答下列问题:
(1)浓硫酸的作用是:①;②;
(2)现拟分离乙酸乙酯、乙酸、乙醇的混合物,下图是分离操作流程图。完成下列空白:
试剂:a______________,b______________。
分离方法:①_____________③_____________
物质名称:A_____________, C_____________
Ⅱ:已知卤代烃(R-X)在碱性条件下可水解得到醇(R-OH),如:CH3CH2-X+H2O  CH3CH2-OH+HR,现有如下转化关系:
CH3CH2-OH+HR,现有如下转化关系:
回答下列问题:
(1)反应1的条件为 __________,X的结构简式为______
(2)写出反应3的方程式______________________。
Ⅲ:写出苹果酸
①和乙醇完全酯化的反应的化学方程式___________________。
②和过量的Na2CO3溶液反应的化学方程式___________________。
下图为实验室制取溴苯的三个装置,根据要求回答下列各题: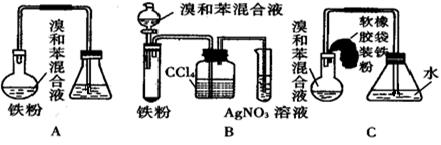
(1)装置A烧瓶中发生反应的化学方程式是;装置A中左侧长导管的作用是;装置A和C中的两处明显错误是、。
(2)在按装置B、C装好仪器及药品后要使反应开始,应对装置B进行的操作是,应对装置C进行的操作是。
(3)装置B、C较好地解决了A中加装药品和使装置及时密封的矛盾,方便了操作。A装置中这一问题在实验中造成的后果是。
(4)B中采用了洗气瓶吸收装置,其作用是。反应后洗气瓶中可能出现的现象是。
(5)B装置也存在两个明显的缺点,其中之一与A、C中的错误相同,而另一个缺点是:。
某化学小组模拟工业生产制取HNO3,设计下图所示装置,其中a为一个可持续鼓入空气的橡皮球。请回答下列问题: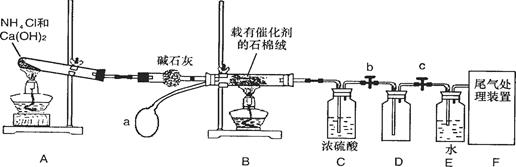
(1)写出装置A中主要反应的化学方程式。
(2)实验结束后,关闭止水夹b、c,将装置D,浸入冰水中,现象是。
(3)装置C中浓H2SO4的作用是。
(4)请你帮助该化学小组设计实验室制取NH3的另一方案。
(5)干燥管中的碱石灰用于干燥NH3,某同学思考是否可用无水氯化钙代替碱石灰,并设计下图所示装置(仪器固定装置省略未画)进行验证。实验步骤如下: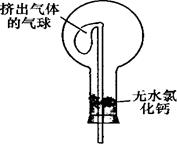
①用烧瓶收集满干燥的氨气,立即塞上如图所示的橡胶塞。
②正立烧瓶,使无水氯化钙固体滑入烧瓶底部,摇动,可以观察到的现象是,由此,该同学得出结论:不能用CaCl2代替碱石灰。
(1-5班必做题)实验室制得的乙炔中常混有H2S、PH3等杂质气体。如图是两学生设计的实验装置,用来测定电石样品中CaC2的纯度,右边的反应装置相同而左边的气体发生装置则不同,分别如Ⅰ和Ⅱ所示。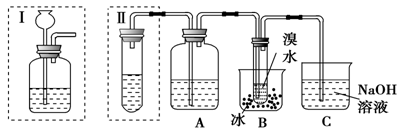
(1)A瓶中的液体可以从酸性KMnO4溶液和CuSO4溶液中选择,应该选择________,它的作用是__。
(2)写出实验室制取乙炔的化学方程式。
(3)装置Ⅰ的主要缺点是_______________。装置Ⅱ的主要缺点是___________________;
若选用Ⅱ装置来完成实验,则应采取的措施是__________________。
(4)若称取m g 电石,反应完全后,测得B处溴水增重n g,则CaC2的纯度为________。
(1-5班必做题)某学生为了验证苯酚、醋酸、碳酸的酸性强弱,设计了如下实验装置,请回答下列问题:
(1)A试管中发生反应的离子方程式。
(2)B试管中的现象是。
(3)该实验设计不严密,请你改正。