(共10分) A、B、C、D、E、F六种短周期元素的原子序数依次增大。
已知A、C、F三原子的最外层共有11个电子,且这种三元素的最高价氧化物的水化物之间两两皆能反应,均能生成盐和水,D元素原子的最外层电子数比次外层电子数少4个,E元素原子的次外层电子数比最外层电子数多3个。试回答:
(1)写出下列元素的符号A ,D ,E 。
(2)用电子式表示B、F形成化合物的过程 。
(3)A、C两种元素最高价氧化物的水化物之间反应的离子方程式
A、B、C、D、E、F、G七种物质间存在如图所示的转化关系,其中A、B、D、G含有同种元素。
已知:
A为金属单质,B为红褐色固体,E为密度最小的气体,G为浅绿色的溶液。
D的水溶液为黄色溶液,能与硝酸银溶液反应生成不溶于稀硝酸的白色沉淀。
在水溶液中D能将某氧化物氧化为F,F是含有三种元素的化合物。
请回答下列问题:
(1)构成C物质的元素在周期表中的位置是,在短周期主族元素中,该元素与其相邻元素的原子半径从大到小的顺序是(用元素符号表示)。
(2)D的水溶液呈性,请用离子方程式解释原因:。
(3)上述反应中属于置换反应的是(填序号)。
(4)反应③(即D将某种氧化物氧化为F)的离子方程式:。
(5)对气体C进行如下实验。已知整个反应过程中,每消耗0.1mol KI,转移的电子数约为3.612×1023个。请按照要求填空:
| 实验步骤 |
实验现象 |
写离子方程式 |
| 将少量气体通入淀粉KI溶液 |
溶液最初变成色 |
|
| 继续通入气体 |
溶液逐渐变成无色 |
下表为元素周期表的一部分,请参照元素①~⑧在表中的位置,用化学用语回答下列问题:
| 周期 |
ⅠA |
0 |
||||||
| 1 |
① |
ⅡA |
ⅢA |
ⅣA |
ⅤA |
ⅥA |
ⅦA |
|
| 2 |
② |
③ |
④ |
|||||
| 3 |
⑤ |
⑥ |
⑦ |
⑧ |
(1)请画出元素⑥的离子结构示意图:。
(2)元素⑦中质子数和中子数相等的同位素符号是:。
(3)④、⑤、⑦的离子半径由大到小的顺序为:。
(4)②的最高价氧化物对应水化物的电离方程式为:。
(5)④、⑤两种元素的原子按1:1组成的常见化合物的电子式为:。
(6)由表中两种元素形成的5核10电子分子常做燃料电池的燃料,该电池在碱性条件下的负极反应式为:。
(7)由表中两种元素形成的氢化物A和B都含有18个电子,A是一种6原子分子,可做火箭发动机燃料;B是一种常见强氧化剂。已知16g液态A与液态B充分反应生成一种液态10电子分子和一种气态单质,并放出838kJ热量,写出A与B反应的热化学方程式:。
我国濒临海域的省份,能够充分利用海水制得多种化工产品。下图是以海水、贝壳(主要成分CaCO3)等为原料制取几种化工产品的工艺流程图,其中E是一种化肥,N是一种常见的金属单质。
结合上述工艺流程回答下列问题:
(1)物质G和L的化学式分别为和;固体B是生活中的一种必需品,主要用作
(2)上述工艺流程中可以循环使用的物质的化学式为
(3)反应①的化学方程式为;在反应①中必须先通入NH3,而后通入D,其原因是
(4)工业上利用F可制得另一种化工产品,该反应的化学方程式为
(5)由K溶液经如何处理才能制得N?
二甲醚(CH3OCH3)是一种重要的精细化工产品,被认为是二十一世纪最有潜力的燃料[ 已知:CH3OCH3(g)+3O2(g)=2CO2(g)+3H2O(1)△H=-1455kJ/mol ]。同时它也可以作为制冷剂而替代氟氯代烃。工业上制备二甲醚的主要方法经历了三个阶段:
①甲醇液体在浓硫酸作用下或甲醇气体在催化作用下直接脱水制二甲醚; 2CH3OH  CH3OCH3+H2O
CH3OCH3+H2O
②合成气CO与H2直接合成二甲醚: 3H2(g)+3CO(g) CH3OCH3(g)+CO2(g)△H=-247kJ/mol
CH3OCH3(g)+CO2(g)△H=-247kJ/mol
③天然气与水蒸气反应制备二甲醚。以CH4和H2O为原料制备二甲醚和甲醇工业流程如下: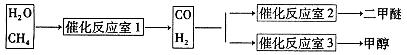
(1)写出CO(g)、H2(g)、O2(g)反应生成CO2(g)和H2O(1)的热化学方程式(结果保留一位小数)
(2)在反应室2中,一定条件下发生反应3H2(g)+3CO(g) CH3OCH3(g)+CO2(g)在密闭容器中达到平衡后,要提高CO的转化率,可以采取的措施是
CH3OCH3(g)+CO2(g)在密闭容器中达到平衡后,要提高CO的转化率,可以采取的措施是
A.低温高压 B.加催化剂 C.增加CO浓度 D.分离出二甲醚
(3)在反应室3中,在一定温度和压强条件下发生了反应:3H2(g)+CO2(g)  CH3OH(g)+H2O (g)△H<0反应达到平衡时,改变温度(T)和压强(P),反应混合物CH3OH“物质的量分数”变化情况如图所示,关于温度(T)和压强(P)的关系判断正确的是(填序号)
CH3OH(g)+H2O (g)△H<0反应达到平衡时,改变温度(T)和压强(P),反应混合物CH3OH“物质的量分数”变化情况如图所示,关于温度(T)和压强(P)的关系判断正确的是(填序号)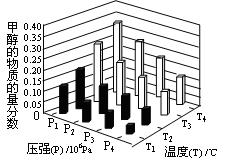
A.P3>P2 T3>T2 B.P2>P4 T4>T2
C.P1>P3 T1>T3 D.P1>P4 T2>T3
(4)反应室1中发生反应:CH4(g)+H2O(g) CO(g)+3H2(g)△H>0写出平衡常数的表达式:
CO(g)+3H2(g)△H>0写出平衡常数的表达式:
如果温度降低,该反应的平衡常数(填“不变”、“变大”、“变小”)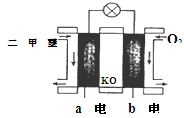
(5)如图为绿色电源“二甲醚燃料电池”的工作原理示意图则a电极的反应式为:________________
(6)下列判断中正确的是_______
A.向烧杯a中加入少量K3[Fe(CN)6]溶液,有蓝色沉淀生成
B.烧杯b中发生反应为2Zn-4eˉ =2Zn2+
C.电子从Zn极流出,流入Fe极,经盐桥回到Zn极
D.烧杯a中发生反应O2 + 4H++ 4eˉ = 2H2O,溶液pH降低
A、B、C、D均为中学化学中常见的单质或化合物,它们之间的关系如图所示(部分产物已略去)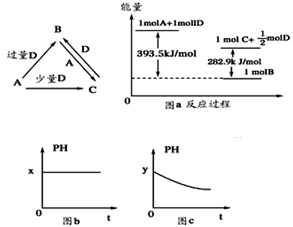
(1)若A为金属单质,D是某强酸的稀溶液,则反应C+D→B的离子方程式为_________
(2)若A、B为盐,D为强碱,A的水溶液显酸性,则 ①C的化学式为___________
②反应B+A→C的离子方程式为____________。
(3)若A为强碱,D为气态氧化物。常温时,将B的水溶液露置于空气中,其pH随时间t变化可能如上图的图b或图c所示(不考虑D的溶解和水的挥发)
①若图b符合事实,则D为________(填化学式),此时图b中x________7(填“﹥”“﹤”“=”)。②若图c符合事实,则其pH变化的原因是_______(用离子方程式表示)
(4)若A为非金属单质,D是空气的主要成分之一。它们之间转化时能量变化如上图a,请写出1molA和D反应生成C的反应热为ΔH=________________