(共8分)常温下,在一刚性容器内部有一个不漏气且可以滑动的活塞,将容器分割成左右两室。左室充入N2,右室充入H2和O2,活塞正好使N2占容器体积的1/4(如图)。然后点燃H2和O2的混合气体,反应完毕后恢复至原来的温度,活塞正好停留在容器的中间。经检验,此时右室中气体可使带火星的木条复燃。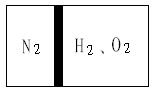
(1)求反应前H2和O2的物质的量之比。
(2)求反应前H2和O2混合气体的平均相对分子质量。
工业上用丁烷氧化法制醋酸,反应的化学方程式可表示为:
2C4H10+5O2 4CH3COOH+2H2O
4CH3COOH+2H2O
现用58吨丁烷为原料制取醋酸,求:
(1)理论上需要标准状况下的空气m3(设空气中O2、N2的体积分数分别为0.2、0.8),同时生成水吨。
(2)若生成的醋酸溶解在生成的水中,所得醋酸的质量分数为%。
(3)若同时生产质量分数为100%的冰醋酸m1吨和质量分数为50%的醋酸m2吨,且 ,需补充水y吨,则y与x的关系式为(用含x的代数式表示y);若不补充水,则m1+m2=。
,需补充水y吨,则y与x的关系式为(用含x的代数式表示y);若不补充水,则m1+m2=。
燃烧法是测定有机化合物分子式的一种重要方法。已知0.1mol某烃A完全燃烧后,生成11.2 L(标准状况)的CO2,生成10.8 g水,回答下列问题。
(1)通过计算推导A的分子式。
(2)写出A可能的结构简式。
将7.8 g过氧化钠与足量的水充分反应,所得溶液的体积为100 mL。试计算:(1)生成氧气的体积(标准状况)。(2)反应后所得溶液中溶质的物质的量浓度。(上述计算均要求写出计算过程)
某有机物0.1mol,与标准状况下5.6L氧气充分反应后,产物为CO、CO2、H2O的混合气体。将此混合气体通过浓硫酸,浓硫酸增重5.4g,再通过灼热氧化铜粉末,氧化铜质量减少1.6g;最后通过足量碱石灰,碱石灰增重8.8g。求该有机物的分子式。(书写计算过程)
将等物质的量A、B混合于2L的密闭容器中,发生如下反应:3A(g)+B(g) xC(g)+2D(g),经5min后,测得D的浓度为0.5mol·L-1,c(A)︰c(B)=3:5,C的平均反应速率是0.1m0L/(L·min)
xC(g)+2D(g),经5min后,测得D的浓度为0.5mol·L-1,c(A)︰c(B)=3:5,C的平均反应速率是0.1m0L/(L·min)
求:(1)反应开始前放入容器中A、B物质的量。(2)B的平均反应速率。(3)x值是多少?