A、B、C、D四种短周期元素原子序数依次增大,A元素原子的价电子排列为ns2np2,B元素的最外层电子数是其电子层数的3倍,E元素原子的价电子排布为3d64s2。C、D的电离能数据如下(kJ·mol―1):
| |
I1 |
I2 |
I3 |
I4 |
| C |
738 |
1451 |
7733 |
10540 |
| D |
577 |
1817 |
2745 |
11578 |
(1)化合价是元素的一种性质。由C、D的电离能数据判断,C通常显 价,D显 价;
(2)某单质甲分子与化合物AB分子中电子总数相等,则甲分子中包含___个σ键,___个π键;
(3)AB的总键能大于甲的总键能,但AB比甲容易参加化学反应。根据下表数据,说明AB比甲活泼的原因是______________________________
| |
单键 |
双键 |
叁键 |
|
| AB |
键能(kJ·mol―1) |
357.7 |
798.9 |
1071.9 |
| 甲 |
键能(kJ·mol―1) |
154.8 |
418.4 |
941.7 |
(4)E能与AB形成配合物,其中E提供______________,AB提供________________。
(5)下列晶胞中,阳离子与阴离子的个数为 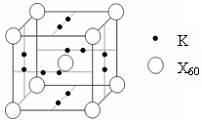
合成氨反应N 2(g)+3H2(g)
2(g)+3H2(g) 2NH3(g),若在恒温、恒压条件下向平衡
2NH3(g),若在恒温、恒压条件下向平衡 体
体 系中通入氩气,平衡移动(填“向左”“向右”或“不”);使用催化剂反应的△H(填“增大”“减小”或“不改变”)。
系中通入氩气,平衡移动(填“向左”“向右”或“不”);使用催化剂反应的△H(填“增大”“减小”或“不改变”)。
浊液中分散质粒子的直径______(填“>”或“<”)100nm,溶液中分散质粒子的直径______(填“>”或“<”)1 nm,而胶体颗粒的直径介于______之间。这个尺寸与现代材料科学中____
nm,而胶体颗粒的直径介于______之间。这个尺寸与现代材料科学中____ __的直径大致相当,从而使胶体的研究更具有现实意义。布朗运动______(“是”或“不是”)胶体的特有性质。
__的直径大致相当,从而使胶体的研究更具有现实意义。布朗运动______(“是”或“不是”)胶体的特有性质。
(1) 按系统命名法命名
①有机物CH3CH(C2H5)CH(CH3)2的名称是________________________。
②在有机物分子中若某一个碳原子连接4个不同的原子或基团,则这种碳原子称为“手性碳原子”。C7H16的同分异构体中具有“手性碳原子”的有两种,名称分别为_____________________、 _____________________。
(2) 写出下列各有机物的结构简式
①2,3-二甲基-4-乙基已烷 _________________________________
②支链只有一个乙基且相对分子质量最小的烷烃___________________
有的油田开采的石油中溶有一种碳氢化合物——金刚烷,它的分子立体结构如图所示: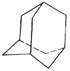
(1)由图可知其分子式为:____________。
(2)它是由_________ 个六元环构成的六体的笼状结构,其中有_________个碳原子为三个环共有,连2个氢原子的碳原子数有个。
(1)写出分子中碳原子数小于10、一氯代物只有一种的所有烷烃的结构简式:
____________、 ____________、 ____________、 ____________。
____________。
(2)由CH3CH2Cl经过3步制乙二醇,写出化学方程式:
①_____________________________________________________
②_____________________________________________________
③_____________________________________________________