KMnO4是一种常用的强氧化剂,工业上可以以软锰矿(主要成分MnO2,另含Al2O3、SiO2杂质)为原料,通过液相法生产。即在碱性条件下用氧气氧化MnO2得到K2MnO4,分离后得到K2MnO4,再用铂板作阳极,铁作阴极电解K2MnO4溶液得到KMnO4,简略生产过程如下所示:
回答下列问题:
(1)写出反应器中反应的方程式
(2)生产过程中最好使用含MnO280%以上的富矿,因为MnO2含量最低的贫矿会导致KOH消耗量偏高,用离子方程式表示KOH消耗偏高的原因 、
。
(3)写出电解槽中阴极和阳极的电极反应方程式
阴极: ;阳极: 。
在电解法中循环Ⅰ、Ⅱ中利用的共同物质是 。
(4)在传统工艺中,得到K2MnO4后,向其中通入CO2制备KMnO4,配平方程式:
K2MnO4+ CO2= KMnO4+ MnO2+ K2CO3
与传统法相比,液相法的优点是:__ _________。
研究工业废弃物的处理和防治具有重要的意义。
(1)利用反应CH4+2NO2 N2+CO2+2H2O可消除NO2的污染,该反应中氧化剂是____,当消耗CH4的体积是11.2 L(标准状况下)时,理论上可处理____molNO2。
N2+CO2+2H2O可消除NO2的污染,该反应中氧化剂是____,当消耗CH4的体积是11.2 L(标准状况下)时,理论上可处理____molNO2。
(2)治理汽车尾气中CO和NO的一种方法是:在汽车排气管中安装一个催化转化装置,该装置能将CO和NO转化为参与大气循环的无毒气体。该反应的化学方程式为________________.
(3)某无色废水中可能含有Fe3+、Al3+、Na+、Cl-、OH-、SO42-、中的几种离子。分别取三份废水进行如下实验:
I.进行焰色反应实验,火焰为无色。
Ⅱ.取100 mL废水,加入足量的BaCl2溶液,生成2.33g白色沉淀。
Ⅲ.取100 mL废水,逐滴加入1.0 mol 的NaOH溶液,消耗NaOH溶液的体积与生成沉淀的质量如下图所示。
的NaOH溶液,消耗NaOH溶液的体积与生成沉淀的质量如下图所示。
请根据上述信息回答下列问题:、
①该废水中一定不含有的离子是__________.
②实验中需配制1.0 mol 的NaOH溶液100 mL,所需仪器除了玻璃棒、托盘天平、量筒、药匙、烧杯、胶头滴管,还缺少的仪器有_______。
的NaOH溶液100 mL,所需仪器除了玻璃棒、托盘天平、量筒、药匙、烧杯、胶头滴管,还缺少的仪器有_______。
③写出图中A→B反应的离子方程式:_______________________。
④通过计算,该废水中______Cl-(填“含有”或“不含有”);若含有,则c(Cl-)=________(若不含有,此问不必作答)。
用电化学原理研究金属铝具有重要的意义。
(1)已知: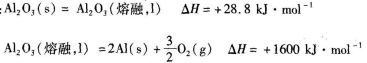
①工业上利用惰性电极电解熔融的Al2O3冶炼铝,每消耗1000kJ电能时,生成27g铝,则电解过程中能量利用率为____。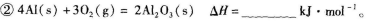
③利用Al2O3制备无水AlCl3的反应为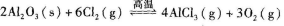
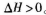 。反应达平衡时,加入焦炭能使平衡向正反应方向移动,理由是__________.
。反应达平衡时,加入焦炭能使平衡向正反应方向移动,理由是__________.
(2)为了防止钢材腐蚀,常采用电解熔融盐法在钢材表面镀铝。熔融盐中铝元素和氯元素仅以 形式存在。如下图所示:
形式存在。如下图所示: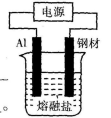
①钢材表面镀铝时,铝应接电源的________极。
②试分析电镀铝时不用氯化铝水溶液作电解液的原因:_______________.
(3)铝一空气-NaOH溶液组成的铝电池性能优越,可用于电动汽车。写出该电池的负极电极反应式______:
(4)铝可用于处理银器表面的黑斑(Ag2S)。将银器置于铝制容器里的食盐水中并与铝接触,形成原电池,可将Ag2S转化为Ag,该过程中食盐水的作用为_______________.
食醋(主要成分CH3COOH )、纯碱(Na2CO3 )和小苏打(NaHCO3 )均为家庭厨房中常用的物质。已知:
请回答下列问题:
(1)定温度下,向0.1 mol CH3COOH 溶液中加入少量CH3COONa 晶体时,下列说法正确的是____(填代号)。
CH3COOH 溶液中加入少量CH3COONa 晶体时,下列说法正确的是____(填代号)。
a.溶液的pH增大b.CH3COOH的电离程度增大
c.溶液的导电能力减弱d.溶液中c(OH- ).c(H+)不变
(2)25℃时,0.10 mol Na2CO3溶液的pH=11,则溶液中由水电离出的c(OH-):_____mol
Na2CO3溶液的pH=11,则溶液中由水电离出的c(OH-):_____mol  。
。
(3)常温下,将20 mL 0.10 mol  CH3COOH溶液和20 mL 0.10 mol
CH3COOH溶液和20 mL 0.10 mol HNO2溶液分别与20 mL 0.10 mol
HNO2溶液分别与20 mL 0.10 mol NaHCO3溶液混合(混合后溶液体积变化忽略不计)。
NaHCO3溶液混合(混合后溶液体积变化忽略不计)。
①反应开始时,v(CH3COOH)_________v(HNO2)(填“>”、“<”或“:”),原因是_________.
②充分反应后.两溶液中c(CH3COO-)_________c(NO2-)(填“>”、“<”或“=”)。
(4)25 C时,向CH3COOH溶液中加入一定量的NaHCO3,所得混合液的pH=6,则混合液中
C时,向CH3COOH溶液中加入一定量的NaHCO3,所得混合液的pH=6,则混合液中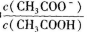 =__________。
=__________。
铜及其化合物在工农业生产及日常生活中应用非常广泛。某研究小组用粗铜(含杂质铁)制备氯化铜晶体(CuCl2.2H2O)的流程如下。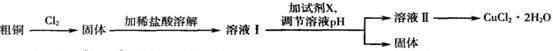
已知常温下,Cu2+、Fe3+的氢氧化物开始沉淀和沉淀完全时的pH见下表:
请回答下列问题:
(1)溶液I中加入试剂X可以调节溶液pH,从而除去Fe3+且不引入杂质。
①试剂X可选用下列物质中的__________(填代号)。
a.CuOb.NaOHc.Cud.Cu(OH)2
②调节溶液pH时,理论上可选择pH最大范围是__________。
(2)由溶液Ⅱ制备CuCl2.2H2O的操作依次为:边滴加浓盐酸边加热浓缩、__________(填操作名称)、过滤、洗涤干燥。
(3)向溶液Ⅱ中通入H2S气体,溶液变浑浊,pH减小,用离子方程式解释其原因:__________.
(4)某学习小组用碘量法测定CuCl2.2H2O样品的纯度(杂质不与发生反应)。实验如下:
a.准确称取CuCl2.2H2O样品mg于小烧杯中,加入适量蒸馏水和足量的碘化钾,再滴入适量的稀硫酸,充分反应后,将所得混合液配成250 mL待测溶液。(已知: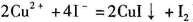 )
)
b.移取25. 00 mL待测溶液于锥形瓶中,加几滴指示剂,用c mol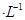 Na2S2O3标准液滴定至终点,重复2次,测得消耗标准液体积的平均值为V mL。 (已知:
Na2S2O3标准液滴定至终点,重复2次,测得消耗标准液体积的平均值为V mL。 (已知: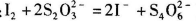 )
)
①实验中使用的指示剂名称为____________。
②达到滴定终点时,仰视滴定管读数将使测定结果_________(填“偏高”、“偏低”或“无影响”)。
③该样品中CuCl2.2H2O 的质量分数为_________(用含m、c、V的代数式表示,不用化简)。
利用“化学蒸气转移法”提纯金属钨的反应原理为:W(s)+I2(g) WI2(g) △H<0
WI2(g) △H<0
(1)该反应的平衡常数表达式K=_________。
(2)在恒温恒容条件下,能够说明上述反应一定达到平衡状态的是_________(填代号)。
a.I2(g)与WI2(g)的浓度相等
b.W的质量不再变化
c.容器内混合气体的密度保持不变
d.容器内混合气体的压强保持不变
(3)在一定温度下,若平衡常数K=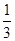 ,向2L恒容密闭容器中加入l mol I2(g)和足量W(s),5 min后反应达到平衡。则0-5 min内的平均反应速率v(WI2)=_________,平衡时I2(g)的转化率为_________。相同温度下,若开始加入I2(g)的物质的量是原来的2倍,则下列数值是原来的2倍的是____(填代号)。
,向2L恒容密闭容器中加入l mol I2(g)和足量W(s),5 min后反应达到平衡。则0-5 min内的平均反应速率v(WI2)=_________,平衡时I2(g)的转化率为_________。相同温度下,若开始加入I2(g)的物质的量是原来的2倍,则下列数值是原来的2倍的是____(填代号)。
a.平衡常数b.达到平衡的时间
c.I2的物质的量浓度d.平衡时WI2的体积分数
(4)为提高该反应的反应速率,同时使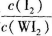 增大,可采取的措施为 ____________.
增大,可采取的措施为 ____________.
(5)工业上利用上述反应原理提纯金属钨的示意图如下: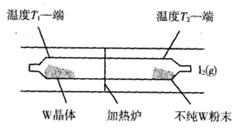
反应在石英真空管中进行,先在温度为T2的一端放入未提纯的W粉末和少量I2(g),一段时间后,在温度为T1的一端得到了纯净的晶体,则温度T1_________T2(填“>”‘<”或“=”)。上述反应体系中循环使用的物质是_________.