超音速飞机在平流层飞行时,尾气中的NO会破坏臭氧层。科学家正在研究利用催化技术将尾气中的NO和CO转变成CO2和N2,化学方程式如下:
2NO+2CO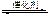 2CO2+N2
2CO2+N2
为了测定在某种催化剂作用下的反应速率,在某温度下用气体传感器测得不同时间的NO和CO浓度如表: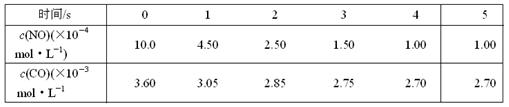

 请回答下列问题(均不考虑温度变化对催化剂催化效率的影响):
请回答下列问题(均不考虑温度变化对催化剂催化效率的影响): (1)在上述条件下反应能够自发进行,则反应的△H 0(填写“>”、“<”、“ = ”。
(1)在上述条件下反应能够自发进行,则反应的△H 0(填写“>”、“<”、“ = ”。 (2)前2s内的平均反应速率v (N2) = ___________________。
(2)前2s内的平均反应速率v (N2) = ___________________。 (3)在该温度下,反应的平衡常数K = 。
(3)在该温度下,反应的平衡常数K = 。 (4)假设在密闭容器中发生上述反应,达到平衡时下列措施能提高NO转化率的是 。
(4)假设在密闭容器中发生上述反应,达到平衡时下列措施能提高NO转化率的是 。
| A.选用更有效的催化剂 | B.升高反应体系的温度 |
| C.降低反应体系的温度 | D.缩小容器的体积 |
(5)研究表明:在使用等质量催化剂时,增大催化剂比表面积可提高化学反应速率。为了分别验证温度、催化剂比表面积对化学反应速率的影响规律,某同学设计了三组实验,部分实验条件已经填在下面实验设计表中。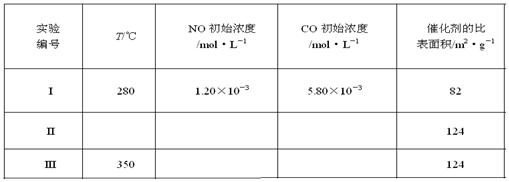
①请在上表格中填入剩余的实验条件数据。
②请在给出的坐标图中,画出上表中的三个实验条件下混合气体中NO浓度随时间变化的趋势曲线图,并标明各条曲线是实验编号。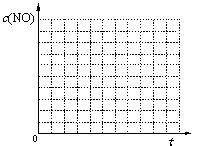
(1)相同物质的量的CO2和O2,原子数目之比为 ,氧原子数目之比为 ;质量相同的CO2和O2,其物质的量之比为 。
(2)20.6 g NaR含有Na+0.2 mol,则NaR的摩尔质量为 g·mol-1,则含R 8.0 g的NaR的物质的量为 mol。
(1)3 mol KClO3完全分解,生成氧气的物质的量为 mol,其质量为 g。
(2) mol Zn和足量的HCl反应,生成氢气1.5 mol。
(3)与5.1 g某二元酸H2R完全反应,刚好消耗NaOH的质量为12 g,则H2R的摩尔质量为 。
(1)0.3 mol NH3分子中所含氢原子数与 个H2O分子中所含氢原子数相等。
(2)含0.4 mol Al3+的Al2(SO4)3中所含的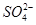 物质的量是 。
物质的量是 。
(3)已知16 g A和20 g B恰好完全反应生成0.04 mol C和31.76 g D,则C的摩尔质量为 。
(4)2.3 g Na是 mol,含 mol e-。
(5)如果ag某气体中含有的分子数为b,则cg该气体的物质的量是(设NA为阿伏加德罗常数) mol。
下列4组物质均有一种物质的类别与其他3种不同:
A.CaO、Na2O、CO2、CuO B.H2、C、P、Cu
C.O2、Fe、Cu、Zn D.H2CO3、H2O、H2SO4、HNO3
(1)以上四组物质中与众不同的物质依次是(填化学式)
A ;B ;C ;D 。
(2)若(1)中四种物质相互作用可生成一种新物质[碱式碳酸铜,化学式Cu2(OH)2CO3],该反应 (填“是”或“不是”)氧化还原反应。
(3)碱式碳酸铜可以看作是Cu(OH)2和CuCO3按照1∶1的比例组成的混合型化合物,写出它与足量盐酸反应的化学方程式:
。
分类方法是研究物质和化学反应的重要方法。
(1)对HCl(盐酸)、H2SO4(硫酸)、HNO3(硝酸)、H3PO4(磷酸)、H2S(氢硫酸)进一步分类时有多种分类角度,请你自定标准进行分类。分类标准是 ,与HCl同属一类的是 。
(2)根据物质的树状分类,PH3的物质类别是 。
A.磷酸盐 B.磷化物 C.氢化物
(3)氧化钙、氢氧化钙分别与盐酸反应的共同点是
,
由此可得出氧化钙属于碱性氧化物。根据上述信息的启示,N2O5与氢氧化钠溶液反应的离子方程式是
。