以CO、H2和CH2=CH2为原料,在钴催化剂作用下加压加热,可制取丙醛: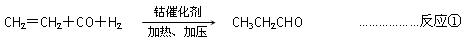
丙醛经反应②(加氢加成)可生成正丙醇、经反应③(催化氧化)可生成丙酸。由正丙醇和丙酸经反应④(酯化反应)生成丙酸正丙酯。请通过计算回答下列问题:
(1)理论上生产3.0 kg正丙醇至少需要标准状况下的氢气 L;
(2)由于副反应的发生,生产中反应①、反应②、反应③的产率分别为80%、80%、90%。若反应④中反应物转化率均为70%。则:
① 以2.8×103kg乙烯为原料,当反应②、反应③中丙醛的投料比为1∶1时,通过上述4步反应最多可制得丙酸正丙酯 kg;
② 反应④中增加正丙醇的投料并保持正丙醇的转化率不变,可以使丙酸的转化率提高20%,此时反应②和反应③中丙醛的投料比应为多少?
向20 mL 0.20 mol/L的NaOH溶液中,缓缓通入一定量的CO2气体,将溶液在一定条件下小心地蒸干,若得到白色固体为纯净物,则通入CO2的体积为________(标准状况).写出反应的离子方程式:___________.
将上述白色固体加水溶解,加盐酸至中性,再蒸干得白色固体,质量为________g.
取50.0 ml Na2CO3和Na2SO4的混合溶液,加入过量BaCl2溶液后得到14.51 g白色沉淀,用过量稀硝酸处理后沉淀量减少到4.66 g,并有气体放出.试计算:
(1)原混合溶液中Na2CO3和Na2SO4的物质的量浓度.
(2)产生的气体在标准状况下的体积.
已知:CuS、Cu2S是两种黑色不溶于水的固体,但一定条件下都能与稀HNO3反应,用离子方程式表示为:
①3CuS+8H++8NO3-=3Cu2++3SO42-+8NO↑+4H2O
②3Cu2S+16H++10NO3-=6Cu2++3SO42-+10NO↑+8H2O
现有不同质量的四份CuS、Cu2S的混合物样品分别和100mL物质的量浓度5mol/L稀硝酸充分反应,所取样品质量与产生气体体积(标准状况下测定)如下表所示:
| 实验序号 |
a |
b |
c |
| 样品质量(g) |
9.6 |
12.8 |
64.0 |
| 气体体积(L) |
5.04 |
6.72 |
V |
试回答下列问题(不考虑硝酸的挥发以及溶液体积变化):
(1)a组实验结束后,溶液中c(NO3-)=;
(2)b组实验结束后,溶液的pH=;
(3)通过计算分析实验c组中产生气体的体积(V)范围。
已知可逆反应:M(g)+N(g) P(g)+Q(g);△H>0,
P(g)+Q(g);△H>0,
请回答下列问题:
(1)在某温度下,反应物的起始浓度分别为:c(M)=" 1" mol·L-1, c(N)="2.4" mol·L-1,达到平衡后,M的转化率为60%,此时N的转化率为 。
(2)若反应温度升高,M的转化率 (填“增大”“减小”或“不变”)。
(3)若反应温度不变,反应物的起始浓度分别为:c(M)=" 4" mol·L-1,c(N)=amol·L-1;达到平衡后,c(P)="2" mol·L-1,a= 。
(4)若反应温度不变,反应物的起始浓度为:c(M)="c(N)=" bmol·L-1,达到平衡后,M的转化率为 。
25.6mg铜与含有1.4×10-3molHNO3的浓硝酸恰好完全反应,放出的气体用排四氯化碳液体的方法收集。
(1)其气体的体积在标准状况下多少?(不考虑生成N2O4)。
(2)将收集到的气体倒立于水槽中,向其中通入标准状况下的O2多少毫升,才能使气体全部生成硝酸?