已知有机物A~F有如图转化关系: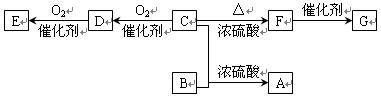
已知:①A的分子式为C8H16O2;
②C分子中只有1个甲基;
③B、E 互为具有相同官能团的同分异构体,且均能与碳酸氢钠反应放出CO2,
④又已知醇在浓硫酸、加热条件下能发生以下类似的反应: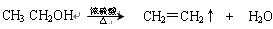
⑤ F能使溴水褪色,G为高分子化合物。
请填写以下空白:
(1)C可能发生的反应有______________________ (填序号)。
①取代反应 ②加成反应 ③加聚反应 ④氧化反应
(2)写出E的结构简式____________________________________________。
写出F与溴的四氯化碳溶液反应生成的有机物的结构简式___________________。
(3)写出下列转化的化学方程式。
B+C→A:_________ C→D:_________ F→G:____________
有一透明溶液,可能含有较大量的Mg2+、Fe3+、Al3+、Cu2+、Na+、H+、SO、CO中的一种或几种,取此溶液做下列实验:①取少量溶液加入用盐酸酸化的BaCl2溶液,有白色沉淀生成;
②取少量溶液加入过氧化钠粉末,溶液中有白色沉淀产生并逸出无色无味的气 体,加入Na2O2的物质的量与析出沉淀的物质的量如图所示。试推断:
体,加入Na2O2的物质的量与析出沉淀的物质的量如图所示。试推断: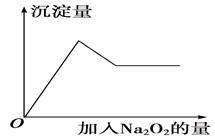
(1)溶液中一定含有的离子是______________ 。
。
(2)溶液中肯定不含有的离子是_______________ _。
_。
(3)可能含有的离子是____________。
A 、B、C、D是四种可溶性化合物,分别由阳离子K+、Ba2+.、Al3+、 Fe3+和阴离子OH—、CO
、B、C、D是四种可溶性化合物,分别由阳离子K+、Ba2+.、Al3+、 Fe3+和阴离子OH—、CO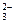 、NO
、NO 、SO
、SO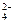 两两组合而成,它们的溶液能发生如下反应:
两两组合而成,它们的溶液能发生如下反应:
(1)A与B反应生成白色沉淀,再加过量A,沉淀量减少,但不会完全消失。
(2)C与D反应生成有色沉淀。
(3)B与C反应生成白色沉淀。
写出它们的化学式:
A._________;B._________;C._________;D._________;
下图为中学化学中常见物质的转化关系,反应条件及部分反应物和产物未全部注明,已知A、D为金属单质,其他为化合物,试推断:
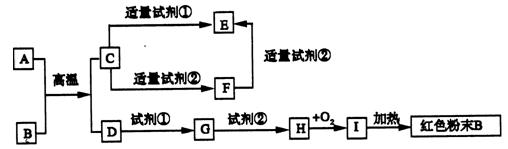
(1)写 出物质的化学式:
出物质的化学式:
(2)写出下列反应的方程式:
C →F的离子方程式:_____________________________________________
→F的离子方程式:_____________________________________________
H→I的化学方程式:______________________________________________
(1) 同期表中位于第8纵行的铁元素属于第________族;
(2) 同期表中最活泼非金属元素位于第________纵行;
(3) 所含元素超过18种的周期是第________、________周期。
I、实验室可利用下列步骤通过“化学放大”来测定极稀的碘化物溶液中I-的浓度:①在中性或弱酸性溶液中,用溴将试样中的I-完全氧化,生成溴化物和碘酸盐,再煮沸以除去过量的Br2;②将所得溶液冷却至室温,加入足量的KI溶液和稀硫酸,充分反应后加入CCl4足量(假设作用完全),再用仪器A将油层分出;③油层用肼(H2N—NH2)的水溶液将CCl4中的I2还原为I-,并进入水溶液中;④水溶液按①法处理;⑤将④所得溶液冷却后加入适量KI溶液并用H2SO4酸化;⑥将⑤所得到溶液取一定量用Na2S2O3标准溶液进行滴定,得出本步骤后溶液中I-的浓度,以此 求出原稀溶液中I-浓度,滴定时的反应为:2Na2S2O3 + I2 = Na2S4O6 + 2NaI。试回答:
求出原稀溶液中I-浓度,滴定时的反应为:2Na2S2O3 + I2 = Na2S4O6 + 2NaI。试回答:
(1)仪器A的名称_____________,如果CCl4用汽油代替,在将油层分出时进行的操作为
______________________________________________________________________________。
(2)如果某试管中有上下两层,均呈无色,采取什么办法判断哪一层是水溶液?
______________________________________________________________________________。
(3)写出离子方程式:
步骤①________________________________________________________;
步骤⑤_______________________________________________。
(4)滴定时,_____________手控制活塞,_____________手摇动锥形瓶。
II、Ag+浓度为0.100 mol·L-1的溶液5 mL,加入等物质的量的某碱金属盐,充分反应后生成卤化物沉淀,经过滤、洗涤后在200 W灯泡下烘干,得到1.297×10-2 g固体。
(5)如果卤化物沉淀为AgX,则其物质的量为_____________mol,根据数据分析上述沉淀是否为AgX沉淀:_ ____________(填“是”或“不是”);若为AgX沉淀,则它的化学式为__________(若不为AgX沉淀,则此空不填)。
____________(填“是”或“不是”);若为AgX沉淀,则它的化学式为__________(若不为AgX沉淀,则此空不填)。
(6)如果卤化物沉淀为碱金属卤化物,其摩尔质量为_____________(计算结果保留整数),根据分析,它的化学式为_____________。