鉴别淀粉、蛋白质、葡萄糖水溶液,依次所用试剂和对应的现象正确的是( )
| A.碘水,变蓝色;浓硝酸,变黄色;新制氢氧化铜,砖红色沉淀 |
| B.浓硝酸,变黄色;新制氢氧化铜,砖红色沉淀;碘水,变蓝色 |
| C.新制氢氧化铜,砖红色沉淀;碘水,变蓝色;浓硝酸,变黄色 |
| D.碘水,变蓝色;新制氢氧化铜,砖红色沉淀;浓硝酸,变黄色 |
核反应可以提供很高能量,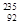 U是重要的核工业原料,在自然界的含量很低。
U是重要的核工业原料,在自然界的含量很低。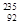 U的浓缩一直为国际社会关注。下列有关
U的浓缩一直为国际社会关注。下列有关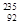 U说法正确的是
U说法正确的是
A.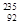 U与 U与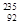 U互为同位素 U互为同位素 |
B.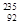 U与 U与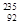 U互为同素异形体 U互为同素异形体 |
C.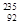 U原子核中含有92个中子 U原子核中含有92个中子 |
D.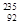 U原子核外有143个电子 U原子核外有143个电子 |
下列性质中,可以证明某化合物内一定存在离子键的是
| A.可溶于水 | B.熔融状态能导电 | C.水溶液能导电 | D.具有较高的熔点 |
下列说法正确的是
| A.Li是最活泼金属元素,F是最活泼非金属元素 |
| B.Mg(OH)2碱性比Ca(OH)2强 |
| C.元素周期表有7个主族,7个副族,1个0族,1个Ⅷ族,共16个纵行 |
| D.X2+的核外电子数目为10, 则X在第3周期第ⅡA族 |
在原电池和电解池的电极上所发生的反应,同属氧化反应或同属还原反应的是
①原电池正极和电解池阳极所发生的反应 ②原电池正极和电解池阴极所发生的反应 ③原电池负极和电解池阳极所发生的反应④原电池负极和电解池阴极所发生的反应
| A.①② | B.①④ | C.②③ | D.③④ |
下列关于化学反应速率的说法正确的是
| A.化学反应速率是指一定时间内任何一种反应物物质的量的减少或任何一种生成物物质的量的增加 |
| B.化学反应速率为0.8 mol·(L·s)-1是指1 s 时某物质的浓度为0.8 mol·L-1 |
| C.根据化学反应速率的大小可以知道化学反应进行的快慢 |
| D.对于任何化学反应来说,反应速率越快,反应现象就越明显 |