将一定量的乙二醇(分子式为C2H6O2)完全燃烧后的所有产物,全部通入过量的石灰水中, 完全被吸收,经过滤得到20g沉淀。滤液的质量比原石灰水的质量减少了(不考虑过滤时液体质量的损失)( )
| A.4g | B.5.8g | C.11.2g | D.14.2g |
PASS是新一代高效净水剂,它由X、Y、Z、W、R五种短周期元素组成,五种元素原子序数依次增大。X原子是所有原子中半径最小的,Y、R同主族,Z、W、R同周期,Y原子的最外层电子数是次外层的3倍,Z是常见的金属,能层数等于主族序数,W单质是人类将太阳能转变为电能的常用材料。下列说法正确的是()
| A.Z与Y形成的化合物可作为耐高温材料 |
| B.WY2能与碱反应,但不能与任何酸反应 |
| C.原子半径按X、Y、Z、R、W的顺序依次增大 |
| D.熔沸点:X2R>X2Y |
如图表示在某溶液中滴加Ba(OH)2溶液时,生成的沉淀的物质的量随Ba(OH)2溶液的体积变化关系。该溶液的成分可能是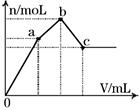
| A.NH4Al(SO4)2 | B.KAl(SO4)2 |
| C.Al2(SO4)3 | D.Na2SO4与NaAlO2组成的混合物 |
C和CuO在一定温度下反应,产物有Cu、Cu2O、CO、CO2。若将2.00 g C跟16.0 g CuO混合,隔绝空气加热,将生成的气体全部通过足量的澄清石灰水,反应一段时间后共收集到1.12 L气体(标准状况),生成沉淀的质量为5.00 g。下列说法错误的是()
| A.反应后的固体混合物中Cu的质量为1 2.8 g |
| B.反应后的固体混合物中还含有碳 |
| C.反应后的固体混合物总质量为14.4 g |
| D.反应后的固体混合物中氧化物的物质的量为0.05mol |
已知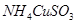 与足量的10mol/L硫酸液混合微热,产生下列现象:①有红色金属生成②产生刺激性气味的气体 ③溶液呈现蓝色。据此判断下列说法正确的是
与足量的10mol/L硫酸液混合微热,产生下列现象:①有红色金属生成②产生刺激性气味的气体 ③溶液呈现蓝色。据此判断下列说法正确的是
| A.反应中硫酸作氧化剂 | B.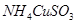 中硫元素被氧化 中硫元素被氧化 |
| C.刺激性气味的气体是氨气 | D.1mol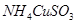 完全反应转移0.5mol电子 完全反应转移0.5mol电子 |
某溶液可能含有Clˉ、SO42-、CO32-、NH4+、Fe3+、Al3+和K+。取该溶液100mL,加入过量NaOH溶液,加热,得到0.02mol气体,同时产生红褐色沉淀;过滤,洗涤,灼烧,得到1.6g固体;向上述滤液中加足量BaCl2溶液,得到4.66g不溶于盐酸的沉淀。
由此可知原溶液中
| A.至少存在5种离子 |
| B.Clˉ一定存在,且c(Clˉ)≥0.4mol/L |
| C.SO42ˉ、NH4+、一定存在,Clˉ可能不存在 |
| D.CO32ˉ、Al3+一定不存在,K+可能存在 |