下列有关实验的做法错误的是
| A.分液时,分液漏斗中的上层液体应由上口倒出 |
| B.用加热的方法可区分碳酸钠和碳酸氢钠两种固体 |
| C.用渗析的方法可除去Fe(OH)3胶体中混有的Cl- |
| D.加入适量的NaOH可除去NaHCO3溶液中混有的少量Na2CO3 |
对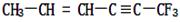 分子结构的下列叙述中,正确的是()
分子结构的下列叙述中,正确的是()
| A.6个碳原子有可能都在同一直线上 |
| B.在同一直线上的原子至少有5个 |
| C.在同一平面上的原子至少有8个 |
| D.分子中呈四面体结构的碳原子有3个 |
设阿伏加德罗常数为NA,下列说法正确的是()
| A.4.4 g乙醛分子中含有的共用电子对数为0.6NA |
| B.标准状况下,11.2 L二氯甲烷所含分子数为0.5 NA |
| C.18.8 g苯酚中含有碳碳双键的个数为0.6 NA |
| D.现有乙烯、丙烯、丁烯的混合气体共14g,其原子数为3NA |
下列有机物命名正确的是( )
A.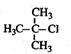 2-甲基-2-氯丙烷 2-甲基-2-氯丙烷 |
B.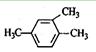 1,3,4-三甲苯 1,3,4-三甲苯 |
C.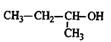 2-甲基-1-丙醇 2-甲基-1-丙醇 |
D.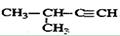 2-甲基-3-丁炔 2-甲基-3-丁炔 |
下列有关化学用语表示正确的是()
A.乙炔的电子式: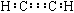 |
B.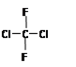 和 和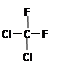 是同一物质 是同一物质 |
C.对甲基苯甲醇的结构简式: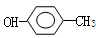 |
D.乙醇分子的比例模型: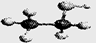 |
化学与生产、生活、科技等密切相关,下列说法正确的是 ( )
| A.石油裂解的目的是提高汽油等轻质油的产量和质量 |
| B.“神州七号”的防护层中含聚四氟乙烯,聚四氟乙烯属于不饱和烃 |
| C.苯酚稀溶液常用于外科消毒,所以自来水也可以用苯酚进行消毒处理 |
| D.煤经气化和液化两个化学变化过程,可变为清洁能源 |