根据下列三个反应的化学方程式,下列关系式正确的是( )
① I2+SO2+2H2O=H2SO4+2HI ② 2FeCl3+2HI=2FeCl2+2HCl+I2 ③ 2FeCl2+Cl2=2FeCl3
| A.氧化性:Fe3+>Cl2>H2SO4>I2 | B.还原性:SO2>I->Fe2+>Cl- |
| C.Fe与I2化合:2Fe+3I2 =2FeI3 | |
| D.FeI2溶液中通入少量的Cl2:2Fe2++2I-+2Cl2=2Fe3++I2+4Cl- |
咖啡酸的结构如图所示,下列说法中错误的是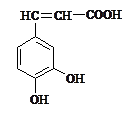
| A.咖啡酸分子中有二种含氧官能团 |
| B.咖啡酸的分子式为C9H5O4 |
| C.咖啡酸可以发生加成、取代、消去等反应 |
| D.1 mol 咖啡酸可与含溶质3mol 的NaOH溶液反应 |
下列叙述中正确的是
| A.电解法精炼铜时,以粗铜作阴极,纯铜作阳极 |
| B.向沸水中滴加FeCl3饱和溶液制备Fe(OH)3胶体 |
| C.常温下,将pH =10的氨水稀释,溶液中所有离子浓度都减小 |
| D.反应NH3(g)+HCl(g)=NH4Cl(s)在室温下可自发进行,则该反应的△H<0 |
短周期元素W、X、Y、Z的原子序数依次增大,且原子最外层电子数之和为14。W的原子半径比X的大,X原子的最外层电子数是内层电子数的2倍,元素Y是地壳中含量最高的金属元素,Z原子的最外层电子数是其电子层数的2倍。下列说法正确的是
| A.元素X的最高价氧化物对应的水化物的酸性比Z的弱 |
| B.元素Y、Z的简单离子的电子层结构相同 |
| C.元素W与Z形成的化合物为共价化合物 |
| D.原子半径由大到小的顺序为:r(Z)>r(Y)>r (W) |
镍镉(Ni-Cd)可充电电池在现代生活中有广泛应用。已知某镍镉电池的电解质溶液为KOH溶液,其充、放电按下式进行:Cd +2NiOOH +2H2O Cd(OH)2+2Ni(OH)2
Cd(OH)2+2Ni(OH)2
有关该电池的说法正确的是
| A.放电时负极得电子,质量减轻 |
| B.放电时电解质溶液中的OH-向负极移动 |
| C.充电时阳极与外加电源的负极相连 |
| D.充电时阴极发生氧化反应 |
下列表示对应化学反应的离子方程式正确的是
| A.氯化铝溶液中加入过量氨水:Al3++4NH3·H2O=AlO2-+4NH4++2H2O |
B.用铜为电极电解饱和食盐水:2Cl—+2H2O Cl2↑+H2↑+2OH— Cl2↑+H2↑+2OH— |
| C.硫酸亚铁溶液被空气中氧气氧化:4Fe2++O2+2H2O=4Fe3++4OH- |
| D.小苏打溶液中加少量Ba(OH)2溶液:2HCO3—+Ba2++2OH—=BaCO3↓+2H2O+CO32— |