短周期元素W、X、Y、Z的原子序数依次增大,且原子最外层电子数之和为14。W的原子半径比X的大,X原子的最外层电子数是内层电子数的2倍,元素Y是地壳中含量最高的金属元素,Z原子的最外层电子数是其电子层数的2倍。下列说法正确的是
| A.元素X的最高价氧化物对应的水化物的酸性比Z的弱 |
| B.元素Y、Z的简单离子的电子层结构相同 |
| C.元素W与Z形成的化合物为共价化合物 |
| D.原子半径由大到小的顺序为:r(Z)>r(Y)>r (W) |
下列有关离子检验的操作和实验结论都正确的是
| 选项 |
实验操作及现象 |
实验结论 |
| A |
向某溶液中加入氯化钡溶液,有白色沉淀生成,再加盐酸酸化,沉淀不溶解 |
该溶液中一定含有SO42— |
| B |
向某溶液中先加入几滴KSCN溶液,再滴入酸性高锰酸钾溶液,溶液变为浅红色 |
该溶液中一定含有Fe2+ |
| C |
在酒精灯上加热铝箔,铝箔熔化,但不滴落,好像有一层膜兜着 |
铝易被氧化;铝的熔点比氧化铝低 |
| D |
向某溶液中加入稀盐酸,产生能使澄清石灰水变浑浊的无色气体 |
该溶液中一定含有CO32— |
某工厂用CaSO4、NH3、H2O、CO2制备(NH4)2SO4,其工艺流程如下: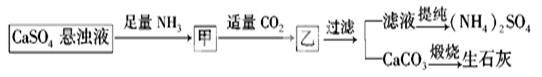
下列推断不合理的是
| A.往甲中通适量CO2有利于(NH4)2SO4生成 |
| B.生成1 mol(NH4)2SO4至少消耗2 molNH3 |
| C.CO2可被循环利用 |
| D.NH3、CO2的通入顺序可以互换 |
利用如图所示装置进行实验,能实现实验目的是(必要时可加热)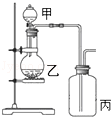
| 选项 |
实验目的 |
甲 |
乙 |
丙 |
| A |
制取并收集NH3 |
浓氨水 |
CaO |
H2O |
| B |
制取并验证碳酸酸性比硅酸强 |
浓盐酸 |
大理石 |
硅酸钠溶液 |
| C |
制取并验证Cl2没有漂白性 |
浓盐酸 |
MnO2 |
干燥的红布条 |
| D |
制取并验证SO2具有漂白性 |
70%硫酸 |
Na2SO3 |
品红试液 |
水溶液中能大量共存的一组离子是
| A.NH4+、Ba2+、Br﹣、CO32﹣ |
| B.Cl﹣、SO32﹣、Fe2+、H+ |
| C.K+、Na+、SO42﹣、MnO4﹣ |
| D.Na+、H+、NO3﹣、HCO3﹣ |
下列表示对应化学反应的离子方程式正确的是
| A.用KIO3氧化酸性溶液中的KI:5I-+IO3-+3H2O=3I2+6OH- |
B.向NH4HSO3溶液中加过量的NaOH溶液并加热:NH4++OH-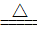 NH3↑+H2O NH3↑+H2O |
| C.将过量SO2通入冷氨水中:SO2+NH3·H2O=HSO3-+NH4+ |
| D.Ba(OH)2溶液中逐滴加入一定物质的量浓度的NaHSO4溶液,当溶液中的OH-恰好反应一半时:Ba2++2OH-+2H++SO42-=BaSO4↓+2H2O |