如图为某有机物的结构简式,每个节点处代表有一个碳原子,与其结合的氢原子的元素符号省略,这种化学式称为“键线式”。又知酯类在铜铬氧化物(CuO·CuCrO4)催化下,与氢气反应得到醇,羰基双键可同时被还原,但苯环在催化氢化过程中不变,其反应原理如下:
关于该化合物的下列说法中,正确的是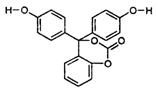
| A.该有机物的化学式为C20H14O5 |
| B.1mol该有机物与浓溴水反应,消耗5molBr2 |
| C.与足量氢氧化钠溶液充分反应,所得产物中相对分子质量较小的钠盐为HCOONa |
| D.1mol该有机物在铜铬氧化物催化下能与2mol氢气发生反应 |
现有四种元素的基态原子的电子排布式如下①1s22s22p63s23p4 ②1s22s22p63s23p3; ③1s22s22p5下列正确的是
| A.第一电离能:③>②>① | B.原子半径:③>②>① |
| C.电负性:③>②>① | D.不成对电子数:③>②>① |
4p轨道电子排布达到半充满的元素,其原子序数是
| A.15 | B.33 | C.35 | D.51 |
气态中性基态原子的原子核外电子排布发生如下变化,吸收能量最多的是
| A.1s22s22p63s23p2→1s22s22p63s23p1 |
| B.1s22s22p63s23p3→1s22s22p63s23p2 |
| C.1s22s22p63s23p4→1s22s22p63s23p3 |
| D.1s22s22p63s23p63d104s24p1 →1s22s22p63s23p63d104s2 |
基态原子的价电子构型3s23p3,下列关于它的描述正确的是
| A.该元素的电负性小于1.8 |
| B.3p能级上的3个电子能量相等,自旋状态相同 |
| C.它的氢化物分子中有四个键合电子 |
| D.该元素的价电子数是4 |
基态硅原子的电子排布图正确的是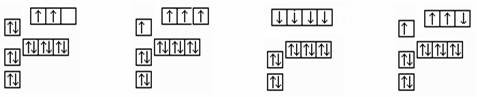
A B C D