根据实验目的判断下列实验操作或装置正确的是
下列化学实验事实及解释都正确的是 ()
| A.碳酸钙不溶于水,所以它是非电解质 |
| B.强电解质的水溶液一定比弱电解质溶液的导电能力强 |
| C.升高温度可以增大单位体积内活化分子的百分数 |
| D.非自发反应在任何条件下都不能实现 |
下列物质在水溶液中的电离方程式书写正确的是()
| A.CH3COOH ="=" H++CH3COO- | B.Na2SO4=== 2Na++SO42- |
C.H2S 2H++ S2- 2H++ S2- |
D.NaHCO3 Na++H++CO Na++H++CO |
下列关于热化学反应的描述中正确的是( )
| A.HCl和NaOH反应的中和热ΔH=-57.3 kJ/mol,则H2SO4和Ba(OH)2反应的中和热ΔH=2×(-57.3) kJ/mol |
| B.CO(g)的燃烧热是ΔH=-283.0 kJ/mol,则2CO2(g)===2CO(g)+O2(g)反应的ΔH=+2×283.0 kJ/mol |
| C.需要加热才能发生的反应一定是吸热反应 |
| D.吸热反应中,新化学键形成吸收能量;放热反应中,新化学键形成放出能量 |
下列说法正确的是()
| A.可逆反应的特征是反应混合物中各组分的浓度相等 |
| B.在其他条件不变时,使用催化剂只能改变反应速率,而不能改变化学平衡状态 |
| C.在其他条件不变时,升高温度可以使平衡向放热反应方向移动 |
| D.在其他条件不变时,增大压强一定会破坏气体反应的平衡状态 |
[化学--修3:物质结构与性质](15分)黄血盐(亚铁氰化钾,K4[Fe(CN)6] )易溶于水,广泛用做食盐添加剂(抗结剂),食盐中黄血盐的最大使用量为10 mg·kg-1。黄血盐经长时间火炒,超过400℃时会分解生成剧毒的氰化钾。回答下列问题:
(1)写出基态Fe2+的核外电子排布式________________________。K4[Fe(CN)6]中Fe2+与CN-两种离子之间的作用力是________________________。
(2)CN-中碳原子的杂化方式为____________;1molCN-中含有π键的数目为________。
(3)金属钾、铜的晶体的晶胞结构如下图(请先判断对应的图),钾、铜两种晶体晶胞中金属原子的配位数之比为________________________。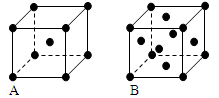
(4)黄血盐溶液与稀硫酸加热时发生非氧化还原反应,生成硫酸盐和一种与CN-是等电子体的气态化合物,反应化学方程式为____________________________________________。