下列哪一组元素的原子间反应可以形成离子键
| 原子 |
a |
b |
c |
d |
e |
f |
g |
||||
| M层电子数 |
1 |
2 |
3 |
4 |
5 |
6 |
7
|
反应产物除与反应物的结构、性质有关,还与反应的条件有关。下列各组物质反应时:
①Cu与HNO3溶液②Cu与FeCl3溶液③Na与O2中,由于浓度或条件不同得到不同产物的是:
| A.①② | B.①③ | C.②③ | D.①②③ |
下列说法中,不正确的是
A.光导纤维的主要成分是SiO2
D.玻璃和陶瓷都属于传统硅酸盐材料
C.明矾和漂白粉均可用于自来水的杀菌、消毒
D.大量排放SO2会引起酸雨
右图5是石英晶体平面示意图,它实际上是立体的网状结构,其中硅、氧原子数之比为.原硅酸根离子SiO44-的结构可表示为左图.二聚硅酸根离子Si2O76-中,只有硅氧键,它的结构可表示为
图所示某硅氧离子的空间结构示意图(虚线不表示共价键)。通过观察分析,下列叙述正确的是()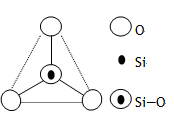
| A.键角为120℃ | B.化学组成为SiO32- | C.键角为60° | D.化学组成为SiO44- |
SF6是一种无色气体,具有很强的稳定性,可用于灭火。SF6的分子结构如图所示,呈正八面体型。如果F元素有两种稳定的同位素,则SF6的不同分子种数为()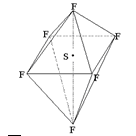
| A.6种 | B.7种 | C.10种 | D.12种 |