“酒是陈的香”,是因为酒在储存过程中生成了有香味的乙酸乙酯。在实验室我们可以用如图所示的装置来制取乙酸乙酯。回答下列问题:
(1)写出试管a中发生的化学方程式:
。
(2)试管b中所盛的溶液为  ,其主要作用是 。
,其主要作用是 。
(3)试管b中的导管要在液面的稍上方,不能插入液面以下,其目的是 。
(4)该实验中,若用3mol乙醇和1mol乙酸在浓硫酸作用下加热,充分反应后,能否生成1mol乙酸乙酯? (填“能”或“不能”)原因是

 。(不考虑原料损耗)。
。(不考虑原料损耗)。
某化学兴趣小组同学以TiO2和CCl4为原料在实验室制取液态TiCl4,装置如图所示。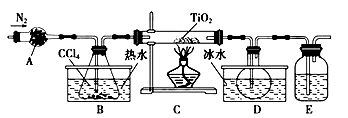
有关信息如下:
①反应原理:TiO2(s)+CCl4(g)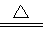 TiCl4(g)+CO2(g)
TiCl4(g)+CO2(g)
②反应条件:无水无氧且加热
③有关物质性质如下表:
请回答下列问题:
(1)B中盛有CCl4的仪器名称是__________,仪器A装的试剂不可能是(填序号)_____________。
a.碱石灰b.无水硫酸铜 c.氧化钙d.烧碱
(2)实验开始前的操作包括:①组装仪器,②_____________,③加装药品,④____________,⑤最后点燃酒精灯。第④步的目的是___________________。
(3)装置E中的试剂是_____________;E装置____________(填“能”或“不能”换成A装置,理由是_______________________。
(4)欲分离D中的液态混合物,所采用操作的名称是__________________。
(5)TiCl4还可由TiO2和焦炭、氯气在加热下反应制得,同时有气体生成,请设计实验方案探究气体的成分。____________________。
用密度为1.84g/mL,质量分数为98%的浓硫酸配制100 ml 3.0mol/L 稀硫酸的实验步骤如下:①计算所用浓硫酸的体积 ②量取一定体积的浓硫酸 ③稀释 ④转移 ⑤洗涤 ⑥定容 ⑦摇匀
(1)所需浓硫酸的体积是 。
(2)第③步实验的操作是 。
(3)第⑥步实验的操作是 。
(4)下列情况对所配制的稀硫酸浓度有何影响?(用字母填写a.偏高 b.偏低 c.无影响)
| A.所用的浓硫酸长时间放置在密封不好的容器中 |
| B.容量瓶用蒸馏洗涤后残留有少量的水 |
| C.所用过的烧杯、玻璃棒未洗涤 |
| D.量取浓硫酸时仰视量筒上的刻度取用浓硫酸 |
E.定容时,滴加蒸馏水,先使液面略高于刻度线,再吸出少量水使液面凹面与刻度线相切
F.定容后摇匀,发现液面降低,又补加少量水,重新达到刻度线
(5)本实验最浪费时间的地方是将稀释后的硫酸冷却至室温,为了节约时间,简单易行的加
快稀硫酸冷却的方法是_____________________。
CH3Cl为无色,略带臭味的气体,密度为2.25g/L,熔点为-24.2℃,20℃时在水中的溶解度为400mL,易溶于乙醇和丙醇等有机溶剂。
Ⅰ.实验室制取CH3Cl的原理是CH3OH +HCl(浓)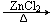 CH3Cl+H2O。具体步骤如下:
CH3Cl+H2O。具体步骤如下:
①干燥ZnCl2晶体;
②称取24g研细的无水ZnCl2和量取20mL浓盐酸放入圆底烧瓶,同时量取一定量的甲醇放入分液漏斗中;
③将分液漏斗里的甲醇逐滴滴入烧瓶中并加热,待ZnCl2完全溶解后有CH3Cl气体逸出,可用排水法收集。请回答:
(1)实验室干燥ZnCl2晶体制得无水ZnCl2的方法是 。
(2)反应过程中滴入烧瓶中甲醇的体积比盐酸少(甲醇与浓盐酸的物质的量浓度接近)
其理由是 。
(3)实验室为何用排水法收集CH3Cl?
Ⅱ.据某资料记载,CH4分子中的一个H原子被Cl原子取代后,其稳定性受到影响,可被强氧化剂酸性高锰酸钾氧化。现有四只洗气瓶;分别盛有以下试剂:
| A.1.5%KMnO4(H+)溶液 | B.蒸馏水 |
| C.5%Na2SO3溶液 | D.98%H2SO4 |
(1)为证实这一理论的可靠性,请从上面选择最恰当的洗气瓶,将a装置生成的气体依次通过洗气瓶
(填洗气瓶编号),如果观察到 则证实上述资料的正确性。
(2)写出洗气瓶中发生反应的离子方程式(C元素的氧化产物为CO2):
(3)如果CH3Cl是大气的污染物,上述洗气瓶之后还应接一只盛 的洗气瓶。
工业上利用硫铁矿烧渣(主要成分为Fe3O4、Fe2O3、FeO、SiO2)为原料制备高档颜料——铁红(Fe2O3),具体生产流程如下:
试回答下列问题:
(1)“酸溶”过程中Fe3O4发生反应的离子反应方程式为 ;
(2)实验室实现“步骤Ⅱ”中分离操作所用的玻璃仪器有 、玻璃棒和烧杯等;步骤Ⅳ中应选用 试剂调节溶液的pH(填字母编号)。
| A.稀硝酸 | B.氢氧化钠溶液 | C.高锰酸钾溶液 | D.氨水 |
(3)检验步骤Ⅲ已经进行完全的试剂是 ;
(4)步骤Ⅴ的反应温度一般需控制在35℃以下,其目的是 ;
(5)步骤Ⅵ中发生反应的化学反应方程式为 ;
(6)步骤Ⅴ中,FeCO3达到沉淀溶解平衡时,若室温下测得溶液的pH为8.5,c(Fe2+)=1×10-6 mol·L-1。试判断所得的FeCO3中是否含有Fe(OH)2 (填“是”或“否”),请通过简单计算说明理由。
(已知:Ksp[Fe(OH)2]=4.9×10-17);
(7)欲测定硫铁矿矿渣中Fe元素的质量分数,称取ag样品,充分“酸溶”、“水溶”后过滤,向滤液中加入足量的H2O2,充分反应后加入NaOH溶液至不再继续产生沉淀,经过滤、洗涤、灼烧至固体恒重,冷却后称得残留固体bg,测得该样品中Fe元素的质量分数为 。
某实验小组用0.50 mol·L-1NaOH溶液和0.50 mol·L-1硫酸溶液进行中和热的测定。
Ⅰ.配制0.50 mol·L-1NaOH溶液
(1)若实验中大约要使用245mLNaOH溶液,至少需要称量NaOH固体 g。
(2)从下图中选择称量NaOH固体所需要的仪器是(填字母): 。
| 名称 |
托盘天平 (带砝码) |
小烧杯 |
坩埚钳 |
玻璃棒 |
药匙 |
量筒 |
| 仪器 |
 |
 |
 |
 |
 |
 |
| 序号 |
a |
b |
c |
d |
e |
f |
Ⅱ.测定稀硫酸和稀氢氧化钠中和热的实验装置如图所示。
(1)写出该反应中和热的热化学方程式:(中和热为57.3 kJ·mol-1) 。
(2)取50 mLNaOH溶液和30 mL硫酸溶液进行实验,实验数据如下表。
| 试验次数 |
起始温度t1/℃ |
终止温度 t2/℃ |
温度差平均值 (t2-t1)/℃ |
||
| H2SO4 |
NaOH |
平均值 |
|||
| 1 |
26.2 |
26.0 |
26.1 |
29.6 |
|
| 2 |
27.0 |
27.4 |
27.2 |
31.2 |
|
| 3 |
25.9 |
25.9 |
25.9 |
29.8 |
|
| 4 |
26.4 |
26.2 |
26.3 |
30.4 |
①上表中的温度差平均值为 ℃。
②近似认为0.50 mol·L-1 NaOH溶液和0.50 mol·L-1硫酸溶液的密度都是1 g·cm-3,中和后生成溶液的比热容c=”4.18” J·(g·℃)-1。则中和热ΔH= (取小数点后一位)。
③上述实验数值结果与57.3 kJ·mol-1有偏差,产生偏差的原因可能是(填字母) 。
a.实验装置保温、隔热效果差
b.量取NaOH溶液的体积时仰视读数
c.分多次把NaOH溶液倒入盛有硫酸的小烧杯中
d.用温度计测定NaOH溶液起始温度后直接测定H2SO4溶液的温度
④实验中改用60mL0.5mol/L盐酸跟50mL0.55moi/L氢氧化钠进行反应,与上述实验相比,所放出的热量 (填相等或不相等,下同),所求的的中和热 简述理由 。