标准状况下,有A、 B、C三种气态烃组成的混合物共xmol,与足量氧气混合点燃完全燃烧后恢复原状况(标准状况)时,气体体积减少了44.8xL,则3种烃可能为
B、C三种气态烃组成的混合物共xmol,与足量氧气混合点燃完全燃烧后恢复原状况(标准状况)时,气体体积减少了44.8xL,则3种烃可能为
A.CH 4 C2H6 C3H8 B.CH4 C2H4 C3H4
4 C2H6 C3H8 B.CH4 C2H4 C3H4
C.C2H4 C 2H2 CH4 D.C2H6 C3H6 C2H2
2H2 CH4 D.C2H6 C3H6 C2H2
1molX气体和amolY气体在体积可变的密闭容器中发生如下反应:
X(g) + aY(g)  bZ(g)反应达到平衡后,测得X的转化率为50%。而且,在同温同压下还测得反应前混合气体的密度是反应后混合气体密度的3/4,则a和b的数值可能是( )
bZ(g)反应达到平衡后,测得X的转化率为50%。而且,在同温同压下还测得反应前混合气体的密度是反应后混合气体密度的3/4,则a和b的数值可能是( )
| A.a=1,b="1" | B.a=2,b="1" | C.a=2,b="2" | D.a=3,b=2 |
在一固定容积的密闭容器中加入2 L X气体和3 L Y气体,同时发生如下反应:nX(g)+3Y(g) 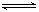 2R(g) +Q(g),反应达到平衡时,测知X和Y的转化率分别为30%和60%。问化学方程式中的n值是()
2R(g) +Q(g),反应达到平衡时,测知X和Y的转化率分别为30%和60%。问化学方程式中的n值是()
| A.1 | B.2 | C.3 | D.4 |
在某条件下,容器中有如下平衡反应:A +4B  2C + D + Q,此时,A,B,C的物质的量均为amol,而D的物质的量为dmol。改变a的取值,再通过改变反应的条件,可以使反应重新达到平衡,并限定达到新的平衡时,D的物质的量只允许在d/2与2d之间变化,则a的取值范围应是__________________________(用a和d的关系式表示)。
2C + D + Q,此时,A,B,C的物质的量均为amol,而D的物质的量为dmol。改变a的取值,再通过改变反应的条件,可以使反应重新达到平衡,并限定达到新的平衡时,D的物质的量只允许在d/2与2d之间变化,则a的取值范围应是__________________________(用a和d的关系式表示)。
在一定条件下,将X和Y两种气体按不同比例充入密闭容器中,并保持其他条件不变,测得平衡时X和Y的转化率与起始状态X与Y的物质的量之比有如右图所示的关系,则X和Y反应的方程式是()
A.2X+Y Z Z |
B.X+2Y Z Z |
C.3X+Y 2Z 2Z |
D.2X+Y 2Z 2Z |
加热N2O5按下式分解:N2O5 N2O3+O2,N2O3又按N2O3
N2O3+O2,N2O3又按N2O3 N2O+O2分解,在容积为1L的密闭容器中,将4molN2O5加热至t℃,达平衡时,氧气的浓度为4.5mol/L,N2O5的平衡浓度为1.7mol/L,则t℃时N2O5的平衡浓度应为()
N2O+O2分解,在容积为1L的密闭容器中,将4molN2O5加热至t℃,达平衡时,氧气的浓度为4.5mol/L,N2O5的平衡浓度为1.7mol/L,则t℃时N2O5的平衡浓度应为()
| A.0.9mol/L | B.1.5mol/L | C.2.38mol/L | D.2.88mol/L |