下表为元素周期表的一部分,请参照元素①-⑧在表中的位置,用化学用语回答下列问题: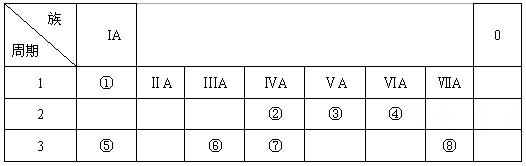

(1)④、⑤、⑥的原子半径由大到小的顺序为_________________________。
(2)②、③、⑦的最高价含氧酸的酸性由强到弱的顺序是_________________________。
(3)①、④、⑤、⑧中的某些元素可形成既含离子键又含极性共价键的化合物,写出其中一种化合物的电子式:____________________。
(4)由表中两种元素的原子按1:1组成的常见液态化合物的溶液易被催化分解,可使用的催化剂为(填序号)_________________。
a.MnO2 b.FeCl3 c.Na2SO3 d.KMnO4
(5)由表中元素形成的常见物质X、Y、Z、M、N可发生以下反应: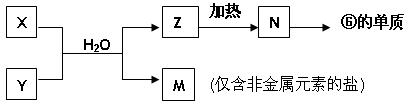
X溶液与Y溶液反应的离子方程式为_______________________________,
N→⑥的单质的化学方程式为______________________________________。
填写下列空白:
(1)34g NH3共有__________mol原子,0.1molH2S共约有____ _个氢原子。同温同压下,等体积的NH3和H2S气体的质量比为____________,含有的分子数目之比为 。等质量的NH3和H2S中分子数目之比为_________。
(2)在标准状况下,35.5g Cl2的体积约是_________L,将其与氢气完全化合生成氯化氢需氢气的物质的量是_________mol,将生成的氯化氢气体溶于1000 g水中,得到密度为a g·cm-3的盐酸,则该盐酸的物质的量浓度是_____________mol/L。
(3)欲配制500mL 0.2mol/L Na2CO3溶液,需要用天平称量Na2CO3·10H2O晶体质量为 。若从配好的上述溶液中取出50mL于一试剂瓶中,需要给它贴上标签,标签上的内容是 ;若再从中取出10mL溶液加水稀释至20mL,则此溶液中Na+的物质的量浓度为 。
Al2(SO4)3的电离方程式为 ,17.1g Al2(SO4)3溶于水配成250mL溶液,SO42-的粒子数为 ,Al3+的物质的量浓度为 。
A、B、C、D、E、F六种短周期主族元素,原子序数依次增大,A、B、F三者原子序数之和为25,且知B、F同主族,1.8g E与足量的盐酸反应生成ECl3和2.24L氢气(标准状况下),D+和E的离子具有相同的电子层结构,工业上用电解元素B和E能形成离子化合物的方法冶炼E单质,试判断:
(1)六种元素中非金属性最强的是 (填代号),该元素位于周期表中第 周期第 族;
由A、B、D三种元素形成化合物的电子式
(2)下列能够说明B、F非金属性强弱的方法有
a.最高价氧化物对应水化物酸性
b.气态氢化物的热稳定性
c.气态氢化物的沸点B比F高
d.向F的气态氢化物溶液中通入B单质,有浑浊
(3)写出下列反应的化学方程式
①E与足量的盐酸反应的化学方程式
②写出足量D的最高价氧化物对应水化物与ECl3相互反应的离子方程式
(一)(1)钠及其化合物是中学化学常用物质,核潜艇或宇宙飞船常用过氧化钠做供氧剂,其原理是_______________________________、_______________________________(用化学方程式表示),若上述变化过程中消耗过氧化钠的质量为23.4g,则变化过程中转移电子数为_____________个。
(2)下列关于Na2O2的叙述正确的是__________
A.Na2O2中阴、阳离子的个数比为1∶1
B.Na2O2分别与水及CO2反应产生相同量的O2时,需要水和CO2的质量相等
C.取a g某物质在O2中完全燃烧,将生成物与足量Na2O2固体完全反应,反应后,固体质量恰好也增加了a g,该物质可能是C6H12O6
D.Na2O2的漂白原理与SO2的漂白原理相同
E.Na2O2与水反应是水作还原剂的氧化还原反应
F.Na2O2与NaHCO3固体按物质的量之比1:1混合加热充分反应后,所得固体中Na2CO3和NaOH的物质的量之比亦为1:1
(二)切开的金属Na暴露在空气中,其变化过程如下:
(1)反应Ⅰ的反应过程与能量变化的关系如右图:
① 反应Ⅰ 是 反应(填“放热”或“吸热”),判断依据是_________________________________。
②1 mol Na(s)全部氧化成Na2O(s)的热化学方程式是 _________________________________。
(2)白色粉末为Na2CO3。将其溶于水配制为0.1 mol/L Na2CO3溶液,下列说法正确的是 (填字母)。
A.升高温度,溶液的pH降低
B.c(OH-)-c (H+)=c (HCO3-)+2 c (H2CO3)
C.加入少量NaOH固体,c (CO32―)与c (Na+)均增大
D.c (Na+) > c (CO32―) > c (HCO3―) > c(OH―) > c (H+)
(3) 钠电池的研究开发在一定程度上可缓和因锂资源短缺引发的电池发展受限问题。
① 钠比锂活泼,用原子结构解释原因___________________________________。
②ZEBRA 电池是一种钠电池,总反应为NiCl2 + 2Na  Ni + 2NaCl。其负极反应式是____________
Ni + 2NaCl。其负极反应式是____________
A、B、C、D、E都是元素周期表中前20号元素,原子序数依次增大,A是地壳中含量最高的元素,B、C、D同周期,E和其他元素既不在同周期也不在同主族,D的氢化物和最高价氧化物对应的水化物均为强酸,且B、C、D的最高价氧化物对应的水化物两两混合均能发生反应生成盐和水。据此回答下列问题:
(1)元素C在元素周期表中的位置是_____________,B的最高价氧化物对应的水化物与D的最高价氧化物混合反应的离子方程式为_________________________________
(2)D的氢化物形成的浓溶液可以使高锰酸钾溶液褪色反应的离子方程式为___________________
(3)A、D、E可以形成多种盐,其中一种盐中A、D、E三种元素的原子个数比为2∶2∶1,该盐的名称为______。它的水溶液与D的氢化物的水溶液反应可生成D的单质,该反应的离子方程式为________。
(4)工业上制取D单质方法的名称是__________,反应的离子方程式是____________________